Süstelahuste lahustid. Süstelahuste valmistamine Süstelahuste lahustid apteegis
Süstimiseks mõeldud ravimvormide hulka kuuluvad vesi- ja õlilahused, suspensioonid ja emulsioonid, samuti steriilsed pulbrid ja tabletid, mis lahustatakse vahetult enne manustamist steriilses lahustis. Kõik need vedelikud viiakse kehasse läbi õõnsa nõela, rikkudes naha ja limaskestade terviklikkust. Sellist vedelike kehasse viimist on kaks vormi - süstimine (injectio) ja infusioon (infusio). Nende erinevus seisneb selles, et esimesed on suhteliselt väikesed vedelikukogused, mida süstitakse süstlaga, ja teised on suured vedelikukogused, mida süstitakse Bobrovi aparaadi või muude seadmete abil. Apteegipraktikas kasutatakse tavaliselt üht üldmõistet – süstimine.
Annustamisvormi omadused
Süstimise tüübid. Sõltuvalt süstekohast eristatakse järgmisi süstetüüpe: intradermaalne (intrakutaanne) (injectiones intracutaneae). Väga väikesed kogused vedelikku (0,2-0,5 ml) süstitakse nahka selle välimise (epidermise) ja sisemise (dermis) kihi vahele; subkutaanne (injectiones subcutaneae). Väikesed kogused vedelikku (1-2 ml) süstimise teel ja alla 500 ml infusioonina süstitakse nahaalusesse rasvkude veresoonte ja närvide poolest suhteliselt vaesetes piirkondades, peamiselt õlgade välispinnal ja abaluualuses (süstidega). Imendumine toimub lümfisoonte kaudu, kust raviained vereringesse jõuavad;
intramuskulaarne (injectiones intramusculares). Väikestes kogustes (kuni 50 ml) vedelikku, tavaliselt 1-5 ml, süstitakse lihaste paksusesse, peamiselt tuharatesse, ülemisse välimisse kvadrandi, mis on kõige vähem rikas veresoonte ja närvide poolest. Imemine raviained toimub lümfisoonte kaudu; intravenoosne (injectiones intrave nosae). Vesilahused koguses 1 kuni 500 ml või rohkem süstitakse otse veenivoodisse, sagedamini kubitaalveeni. Suure koguse lahuse infusioon viiakse läbi aeglaselt (1 tund 120-180 ml). Sageli viiakse see läbi tilguti meetodil (sel juhul süstitakse lahust veeni mitte läbi nõela, vaid läbi kanüüli kiirusega 40–60 tilka minutis); intraarteriaalne (injectiones intraarteriales). Lahused süstitakse tavaliselt reie- või õlavarrearterisse. Raviainete toime avaldub sel juhul eriti kiiresti (1-2 s pärast); tsentraalne seljaaju kanal (injectiones intraarachnoidales, s. injectiones cerebrospinaies, s. injectiones endolumbalis). Väikesed kogused vedelikku (1-2 ml) süstitakse nimmelülide III-IV-V tsooni subarahnoidsesse ruumi (pehme ja arahnoidse membraani vahele).
Harvem kasutatakse muid süstetüüpe: suboktsipitaalne (injectiones suboccipitales), pararadikulaarne (injectiones paravertebrales), intraossaalne, intraartikulaarne, intrapleuraalne jne.
Süstitav annustamisvormid on enamasti tõelised lahused, kuid süstimiseks võib kasutada ka kolloidseid lahuseid, suspensioone ja emulsioone. Intravaskulaarsed süstid võivad olla ainult vesilahused. Õli lahused põhjustada emboolia (kapillaaride ummistus). Intravaskulaarsete süstide jaoks sobivad emulsioonid (tüüp M / B) ja suspensioonid ainult siis, kui nendes dispergeeritud faasi osakeste suurus ei ületa 1 mikronit. Vaseliiniõli lahustina ei sobi isegi intramuskulaarseks ja subkutaanne süstimine, sest see moodustab valusalt resistentseid oleoome (õlikasvajaid).
Süstimismeetodi eelised ja puudused. Annustamisvormide manustamismeetodil on mitmeid eeliseid. Nende hulka kuuluvad: manustatud ravimite toimekiirus; ensüümide hävitava toime puudumine seedetrakti ja maksa raviainete jaoks; ravimainete toime puudumine maitse- ja lõhnaorganitele ning seedetrakti ärritus; manustatud ravimite täielik imendumine; raviaine toime lokaliseerimise võimalus (anesteetiliste ainete kasutamise korral); doseerimise täpsus; annustamisvormi patsiendile manustamise võimalus teadvuseta; vere asendamine pärast olulist kaotust; võimalus valmistada steriilseid ravimvorme edaspidiseks kasutamiseks ampullides).
Annustamisvormide manustamise süstimismeetodi puuduste hulgas on selle valu, mis on pediaatrilises praktikas eriti ebasoovitav; süsti võivad teha ainult meditsiinitöötajad.
Kell intravenoosne manustamine ravimaine siseneb kohe ja täielikult suur ring vereringe, näidates samal ajal maksimaalset võimalikku terapeutilist toimet. Sel viisil määratakse ravimaine absoluutne biosaadavus. Samaaegselt intravenoosne lahus võib olla standardne ravimvorm teistes ravimvormides välja kirjutatud ravimite biosaadavuse määramisel (suhteline biosaadavus).
Süstitavate ravimvormide kasutamine sai võimalikuks tänu tõhusate meetodite leidmisele nende steriliseerimiseks, nende manustamiseks mõeldud seadme (süstla) leiutamisele ja lõpuks spetsiaalsete anumate (ampullide) leiutamisele steriilsete ravimvormide säilitamiseks. Kaasaegses koostises on süstidel väga oluline koht ja enamjaolt need vabastatakse ampullides. Meditsiiniasutuste apteekides moodustavad süstid 30–40% kõigist ekstemporaalselt toodetud ravimvormidest.
Nõuded süstitavatele ravimvormidele
Valmistatud süstelahustele esitatakse järgmised nõuded: mehaanilised lisandid(täielik läbipaistvus); lahuse stabiilsus; steriilsus ja apürogeensus; erinõuded.
Nende nõuete edukas täitmine sõltub suuresti apteekri töö teaduslikult põhjendatud korraldusest. Ühel töökohal on rangelt keelatud üheaegselt valmistada mitut süstelahust, mis sisaldavad erinevaid aineid või samu aineid, kuid erinevas kontsentratsioonis. Süstelahuste valmistamine ei ole võimalik andmete puudumisel: sissetulevate komponentide keemilise ühilduvuse, tootmistehnoloogia, steriliseerimisrežiimi ja ka nende keemilise kontrolli meetodite puudumisel. Tõhusat ja rütmilist tööd hõlbustab kõigi abimaterjalide (mõõtkolvid, silindrid, lehtrid jne) ja abimaterjalide (paberfiltrid, vatt, korgid jne) ratsionaalne paigutamine töökohale, mida saab hõlpsasti tööle võtta ilma pingutus ja ebavajalikud liigutused. Süstitavate ravimvormide valmistamisel on eriti oluline kontsentratsioon ja täpsus.
Mehaaniliste lisandite puudumine. Täielik läbipaistvus süstelahused saavutatakse korraliku filtreerimisega. Väikeste lahuste koguste puhul kasutatakse filtreerimist läbi vatitikuga kurdpaberifiltri. Filtraadi esimesed osad, mis võivad sisaldada hõljuvaid kiudude fragmente, suunatakse tagasi filtrisse.
Klaasfiltrid nr 3 (poori suurus 15–40 µm) on mitmekülgsed ja tootlikumad, töötades kerges vaakumis. Otse viaalidesse filtreerimiseks^ kasutage otsikuid (joonis 22.1). Klaasfiltrid ei oma adsorptsiooniomadusi, ei muuda lahuste värvi (mis tekib läbi paberi filtreerimisel, näiteks fenooli derivaadid) ning neid on lihtne puhastada ja steriliseerida. Suure hulga süstelahuste tootmise korral toimub filtreerimine klaasfiltritega filtreerimisseadmetel.

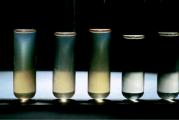
Mehaaniliste lisandite puudumisel kontrollitakse filtreeritud süstelahuseid visuaalselt pärast viaalidesse täitmist, samuti pärast steriliseerimist. Puhtuse visuaalseks kontrolliks kasutatakse seadet UK-2 (joonis 22.2). UK-2 koosneb illuminaatoriga (1), reflektorist (2) ja ekraanist (3) korpusest, mis on monteeritud nagidega (4) alusele. Ekraani saab pöörata ümber vertikaaltelje ja fikseerida soovitud asendisse. Ekraani üks tööpind on värvitud musta emailiga, teine - valge värv. Valgusallikaks on kaks lambipirni võimsusega 40-60 vatti. Lahused on palja silmaga nähtavad. Kontrolleri silmade kaugus viaalist peab olema 25 cm. Kontrolleri nägemisteravus peab olema 1 (kompenseerituna prillidega). Steriilsetes süstelahustes ei tohi visuaalselt tuvastada nähtavaid mehaanilisi lisandeid.
Süstelahuste stabiilsus. Süstelahuste stabiilsuse all mõistetakse nende koostise ja ravimainete koguse muutumatust lahuses tähtajad ladustamine. Süstelahuste stabiilsus sõltub eelkõige algsete lahustite ja ravimainete kvaliteedist. Need peavad täielikult vastama GFH või GOST nõuetele. Mõnel juhul on ette nähtud süstimiseks mõeldud ravimite spetsiaalne puhastamine. See kehtib eriti süstelahuse heksametüleentetraamiini kohta. Glükoosil, kaltsiumglükonaadil, kofeiin-naatriumbensoaadil, naatriumbensoaadil, naatriumvesinikkarbonaadil, naatriumtsitraadil, eufilliinil, magneesiumsulfaadil ja mõnel muul peaks samuti olema kõrgem puhtusaste, st mida kõrgem on preparaatide puhtus, seda stabiilsemad on saadud lahused. neilt süstimiseks.
Raviainete muutumatus saavutatakse ka optimaalsete steriliseerimistingimuste (temperatuur, aeg) järgimisega, vastuvõetavate säilitusainete kasutamisega, mis võimaldavad saavutada soovitud steriliseerimisefekti madalamal temperatuuril, ning ravimainete olemusele vastavate stabilisaatorite kasutamisega.
Parenteraalsete lahuste oluline stabiliseeriv tegur on vesinikioonide optimaalne kontsentratsioon. Parenteraalsete lahuste pakkimisest rääkides viidati, et lahustuvate silikaatide leostumine klaasist ja nende hüdrolüüs toob kaasa pH väärtuse tõusu. Sellega kaasneb paljude ainete lagunemine, eelkõige alkaloidi aluste sadestus. Seetõttu peab alkaloidsoolade stabiilsuse tagamiseks nende lahustel olema teatud pH väärtus. Samuti on kindlaks tehtud, et selliste ühendite nagu atropiin, kokaiin molekulides esinevate estrirühmade seebistumine väheneb pH langusega järsult. Nii et pH 4,5-5,5 juures saab nende ainete lahuseid steriliseerida mitte ainult voolava auruga, vaid ka autoklaavis. PH alandamine stabiilsuse saavutamiseks nõuab ka mõnede organpreparaatide (adrenaliin, insuliin), glükosiidide jne lahuseid.
Optimaalne vesinikioonide kontsentratsioon süstelahustes saavutatakse stabilisaatorite lisamisega, mis on ette nähtud farmakopöa artiklites. Eespool käsitletud juhtudel kasutatakse ravimite, mis on nõrkade aluste ja tugevate hapete soolad, stabiliseerimiseks GPC järgi sagedamini 0,1 n. vesinikkloriidhappe lahus koguses tavaliselt 10 ml 1 liitri stabiliseeritava lahuse kohta. Sel juhul nihkub lahuse pH happepoolele pH väärtuseni 3,0. Vesinikkloriidhappe lahuste kogused ja kontsentratsioonid võivad varieeruda.
Stabilisaatoritena kasutatakse ka leeliselahuseid (seebikivi, naatriumvesinikkarbonaat), mida tuleb lisada ainete lahustesse, mis on tugevate aluste soolad ja nõrgad happed(kofeiin-naatriumbensoaat, naatriumnitrit, naatriumtiosulfaat jne). Nende stabilisaatorite poolt loodud leeliselises keskkonnas on nende ainete hüdrolüüsireaktsioon maha surutud.
Mõnel juhul on kergesti oksüdeeruvate ainete, näiteks askorbiinhappe stabiliseerimiseks vaja lahustesse viia antioksüdante – aineid, mis on palju kergemini oksüdeeruvad kui raviained (naatriumsulfit, naatriummetabisulfit jne).
Mõned süstelahustes olevad ravimained stabiliseeritakse spetsiaalsete stabilisaatoritega (näiteks glükoosilahused). Teave stabilisaatorite koostise ja nende koguste kohta on toodud ametlikus steriliseerimistabelis.
Steriilsus ja apürogeensus. Süstelahuste steriilsus tagatakse aseptiliste tootmistingimuste, kehtestatud steriliseerimismeetodi, temperatuurirežiimi, steriliseerimisaja ja söötme pH range järgimisega.
Üksikute ravimainete lahuste steriliseerimise meetodid ja tingimused on toodud ametlikus steriliseerimise koondtabelis, mis sisaldab üle 100 nimetuse süstelahuseid. Lahuste steriliseerimine peaks toimuma hiljemalt 1-1,5 tundi pärast nende valmistamist. Lahuste, mille maht on üle 1 liitri, steriliseerimine ei ole lubatud. Samuti ei ole lubatud lahuste uuesti steriliseerimine.
Süstelahuste apürogeensus tagatakse pürogeenivaba vee (Aqua pro injectionibus) saamise ja säilitamise reeglite ning süstelahuste valmistamise tingimuste järgimise reeglite range järgimisega.
Erinõuded süstelahustele. Teatud süstelahuste rühmade erinõuete hulgas on järgmised: isotoonilisus, isoioonsus, isohüdrilisus, viskoossus ja muud füüsikalis-keemilised ja bioloogilised omadused, mis saadakse lisaainete (lisaks ravimitele) lahusesse lisamisel.
Loetletud nõuetest apteegipraktikas on sagedamini vaja lahendada süstelahuste isotoniseerimisega seotud küsimusi. Isotooniliste lahuste all mõistetakse lahuseid, mille osmootne rõhk on võrdne kehavedelike osmootse rõhuga: vereplasma, pisaravedelik, lümf jne. Vere ja pisaravedeliku osmootset rõhku hoitakse tavaliselt 7,4 atm juures. Madalama osmootse rõhuga lahuseid nimetatakse hüpotoonilisteks, kõrgema osmootse rõhuga lahuseid hüpertoonilisteks. Süstelahuste isotoonilisus on väga oluline omadus. Vereplasma osmootsest rõhust kõrvalekalduvad lahused põhjustavad tugevat valutunnet ja see on mida tugevam, seda teravam on osmootne erinevus. On teada, et anesteetikumide kasutuselevõtuga (hambaarsti- ja kirurgiapraktikas) põhjustab osmootne trauma pärast anesteesiat tugevat valu, mis kestab tunde. Tundlikud kuded silmamuna nõuavad ka rakendatud lahuste isotoniseerimist. Eelnev ei kehti juhtudel, kui ravi eesmärgil kasutatakse ilmselgelt hüpertoonseid lahuseid (näiteks kudede turse ravis kasutatakse kõrge hüpertoonilise toimega glükoosilahuseid).
Ravimite isotoonilisi kontsentratsioone lahustes saab arvutada erineval viisil. Enamik lihtsal viisil on naatriumkloriidi isotooniliste ekvivalentide arvutamine.
Aine isotooniline ekvivalent naatriumkloriidi mõistes on naatriumkloriidi kogus, mis samadel tingimustel tekitab osmootse rõhu, mis on võrdne 1 g selle raviaine osmootse rõhuga. Näiteks 1 g veevaba glükoosi võrdub osmootse toimega 0,18 g naatriumkloriidiga. See tähendab, et 1 g veevaba glükoosi ja 0,18 g naatriumkloriidi isotoniseerivad sama koguse vesilahuseid.
GPC pakub suhteliselt paljude ravimainete kohta naatriumkloriidi isotooniliste ekvivalentide tabelit, mida on praktikas mugav kasutada. Näiteks kui apteeki saab retsepti 22.1, selgub näidatud tabeli järgi, et dikaiini naatriumkloriidi ekvivalent on 0,18. Üks naatriumkloriid isotoniseerimiseks vajaks 0,9. Saadaolev 0,3 g dikaiini on võrdne: 0,3 x 0,18 \u003d 0,05 g naatriumkloriidiga. Seetõttu tuleb naatriumkloriidi võtta 0,9–0,05 \u003d 0,85.
22.1.Rp.: Solutionis Dicaini 0,3:100 ml
Natrii chloridiq. s.,
ut fiat solutio isotonica
D.S. 1 ml 3 korda päevas subkutaanselt
Füsioloogilistele ja verd asendavatele lahustele esitatakse lisaks isotoonilisusele mitmeid nõudeid. Need lahused on kõige keerulisem süstelahuste rühm. Füsioloogilised lahused on sellised, mis vastavalt lahustunud ainete koostisele on võimelised toetama rakkude ja elundite elutegevust ega põhjusta olulisi muutusi organismi füsioloogilises tasakaalus. Lahuseid, mis on oma omadustelt võimalikult lähedased inimese vereplasmale, nimetatakse verd asendavateks lahusteks (vedelikeks) või vereasendajateks. Füsioloogilised lahused ja vereasendajad peaksid olema eelkõige isotoonilised, kuid lisaks peavad need olema isooonsed, st sisaldama kaalium-, naatrium-, kaltsium- ja magneesiumkloriide vereseerumis omases vahekorras ja kogustes.
Füsioloogilised lahused ja vereasendajad peavad lisaks isotooniale ja isoiooniale vastama ka isohüdria nõuetele, st olema lahuse pH-ga võrdne vereplasma pH-ga (vere pH 7,36). Samas on väga oluline, et neil oleks võime hoida vesinikioonide kontsentratsiooni samal tasemel. Veres saavutatakse see püsivus puhvrite (reaktsiooniregulaatorite) olemasoluga karbonaatsüsteemi (vesinikkarbonaat ja karbonaat), fosfaatsüsteemi (primaarsed ja sekundaarsed fosfaadid) ja valgusüsteemide kujul, mis on oma olemuselt amfolüüdid ja võivad seetõttu säilitavad nii vesiniku- kui hüdroksüülioone. Analoogiliselt verega viiakse vereasendajatesse ja füsioloogilistesse lahustesse vastavaid pH regulaatoreid, mille tulemusena muutuvad need isohüdroksüülseteks.
Füsioloogilised lahused ja vereasendajad sisaldavad tavaliselt glükoosi, et tagada rakkude toitmine ja luua vajalik redokspotentsiaal. Selle kogus veres määratakse tavaliselt 3,88-6,105 mmol / l. Lahuste füüsikalis-keemiliste omaduste lähendamiseks vereplasmale lisatakse neile mõningaid kõrgmolekulaarseid ühendeid. Viimased on vajalikud soolalahuse viskoossuse ja vere viskoossuse võrdsustamiseks. Lisaks kõigele eelnevale peavad verd asendavad vedelikud olema ilma toksiliste ja antigeensete omadusteta, samuti ei tohi need vähendada vere hüübimist ega põhjustada erütrotsüütide aglutinatsiooni.
Süstelahuste eratehnoloogia
Süstelahused valmistatakse massi-mahu kontsentratsioonis. Vajalik kogus ravimit kaalutakse ja lahustatakse mõõtekolvis vees, misjärel lahus reguleeritakse veega vajaliku mahuni. Mahumõõteriistade puudumisel arvutatakse veekogus etteantud kontsentratsiooniga lahuse tiheduse või mahupaisumisteguri väärtuse järgi (vt tabel 8.2).
Ainete lahused, mis ei talu steriliseerimist. Aseptilised töötingimused on piiratud selliste ravimainete süstelahuste valmistamisel, mis ei talu termilist steriliseerimist (barbamiil, medinal, adrenaliinvesinikkloriid, füsostigmiinsalitsülaat, eufilliin) või kui nende lahused ise on bakteritsiidse toimega (kloorpromasiin, diprasiin, heksametüleentetramiin) . Kloorpromasiini ja diprasiini süstelahuste valmistamisel on ka teisi omadusi, kuna neil ainetel on lokaalne ärritav toime ja need põhjustavad dermatiiti. Nendega töötamine peaks toimuma veojõu all, kummikinnastes ja marli sidemetes; analüüsilahus tuleks pipetti võtta ainult pirni abil; pärast tööd tuleb käsi ilma seebita pesta ainult külma veega, eelistatavalt hapendatud.
GPC-s on üldine märge, et kui kuumutamisel lagunevatest ainetest on vaja kiiresti valmistada steriilne lahus, valmistatakse ravimvorm aseptiliselt, lisades 0,5% fenooli või 0,3% trikresooli või küllastunud lahuses. klorobutanoolhüdraadi lahus. Sellised lahused sukeldatakse vette ja kuumutatakse temperatuurini 80 ° C. Sellel temperatuuril jätkatakse kuumutamist vähemalt 30 minutit. Seda juhist ei tohiks laiendada heksametüleentetramiini lahustele, mis steriliseeruvad ise. Aseptiliselt valmistatud lahused väljastatakse sildiga "Aseptiliselt valmistatud".
22.2. Rp.: Lahus on heksametüleentetramini 40% 100 ml
steriliseerimine!
D.S. IV mitte 20 ml 3 korda päevas
Kui mõõteriistu pole, siis tehakse arvutus. Heksametüleentetramiini 40% lahuse tihedus on 1,088 g / cm3, 100 ml seda lahust kaalub: 100 x 1,088 \u003d 108,8 ml, seega on vee kogus: 108,8 - 40 \u003d 68 ml.
Teine arvutusviis: heksametüleentetraamiini mahu suurenemise koefitsient on 0,78, st 1 g lahustamisel suureneb selle vesilahuse maht 0,78 ml; ja 40 g lahustamisel 0,78 x 40 \u003d 31,2. Seetõttu on vaja süstevett: 100–31,2 = 68,8 ml.
Steriliseeritud stendis aseptilistes tingimustes mõõdetakse 68,8 ml süstevett, kaalutakse 40 g heksametüleentetramiini ja lahustatakse statiivis ravim. Lahus filtreeritakse kolbi.
Eufilliini lahused. Eufilliin on väga nõrga happe (teofülliini) ja nõrga aluse (etüleendiamiin) kaksiksool. Sel põhjusel valmistatakse Eufillini süstelahused süsihappegaasivaba vee peal. Vett keedetakse vahetult pärast destilleerimist 30 minutit enne kasutamist. Viaale kasutatakse ainult neutraalsest klaasist. Ravimi kvaliteet peab vastama GFH lisanõuetele. Eufillin süstelahused: 12% lahused ei võimalda kuumsteriliseerimist; ettenähtud 2,4% lahuseid saab steriliseerida voolava auruga (100 °C) B 30 minutit.
Kloorpromasiini lahused. Aminasiini (nagu ka diprasiini) vesilahused oksüdeeruvad kergesti isegi lühiajalisel kokkupuutel valgusega ja moodustuvad punased lagunemissaadused. Sel põhjusel lisatakse nende ainete stabiilse lahuse saamiseks 1 liitri lahuse kohta 1 g veevaba naatriumsulfiti ja metabisulfiti, 2 g askorbiinhapet ja 6 g naatriumkloriidi. Selles lahuses ei mängi askorbiinhape raviaine, vaid antioksüdandi rolli, kuna see, olles oksüdeerunud kiiremini kui aminasiin, kaitseb viimast lagunemise eest. Naatriumkloriidi lisatakse isotooniliseks muutmiseks. Annustamisvorm valmistatakse rangelt aseptilistes tingimustes ilma termilise steriliseerimiseta.
Steriliseerimist taluvate ainete lahused. Enamik süstelahuseid valmistatakse termilise steriliseerimise teel. Steriliseerimismeetodi valik sõltub ravimainete termilise stabiilsuse astmest.
Naatriumvesinikkarbonaadi lahused. Elustamiseks (kliinilise surmaga), atsidoosiga, vere hemolüüsiga, soolade tasakaalu reguleerimiseks jne on ette nähtud 3-5% lahused. Naatriumvesinikkarbonaadi lahuse tehnoloogial on oma omadused. Läbipaistvate lahuste saamiseks, mis on stabiilsed 1 kuu jooksul, on vaja: kasutada kõrge puhtusastmega naatriumvesinikkarbonaati (keemiliselt puhas ja analüütiliselt puhas vastavalt standardile GOST 4201-79); lahustamine tuleb läbi viia suletud anumas temperatuuril mitte üle 15-20 ° C, vältides lahuse loksutamist. Pärast filtreerimist ja analüüsimist valatakse lahus neutraalsetesse klaaspudelitesse (korkimine - metallkorkidega sissejooksmiseks mõeldud kummikorgid) ja steriliseeritakse voolava auruga temperatuuril 100 °C 30 minutit või temperatuuril 119–121 °C 8–12 minutit. Rebenemise vältimiseks täidetakse viaalid ainult 2/3 mahust lahusega; lahuseid tuleks kasutada pärast täielikku jahutamist (et steriliseerimisel eralduv süsinikdioksiid lahustuks).
22.3. Rp.: Amidopürini 2.0
Coffeini-natrii benzoatis 0,8
Novocaini 0,2
Aquae pro injektsioon 20 ml
steriliseerimine!
D.S. 1 ml 3 korda päevas intramuskulaarselt
Kompleksse süstelahuse valmistamisel on mitmeid funktsioone. Kolbi lisatakse amidopüriin, kofeiin-naatriumbensoaat, novokaiin, lisatakse vesi (võttes arvesse FSC-d, kuna tahkete ainete kogus on 15%), suletakse korgiga, kastetakse keevasse vette. veevann ja jätke järk-järgult segades, kuni koostisosad on täielikult lahustunud. Seejärel hoitakse selget lahust veel 3-5 minutit keevas vannis. Lahus filtritakse jaotusviaali, suletakse hermeetiliselt ja steriliseeritakse voolava auruga 30 minutit. Enne kasutamist kontrollitakse lahuse setete puudumist, mis mõnikord tekib amidopüriini osalise sadestumise tõttu, kuna lahus on amidopüriini (1:10) sisalduse poolest üleküllastunud (amidopüriini lahustuvus on 1:20) . Kui tekib sade, lahus kuumutatakse sisse kuum vesi kuni sademe täieliku lahustumiseni ja rakendada jahutatuna temperatuurini 36-37 °C.
Vaatleme näiteid süstelahuste valmistamisest, mille tehnoloogiat raskendab stabiliseerimise ja isotoniseerimise vajadus.
22.4. Rp.: Securinini nitratis 0,2
Salution Acid vesinikkloriidhape 0,1 N 0,5 ml
Aquae pro injectionibus ad 100 ml
steriliseerimine!
D.S. 1 ml 1 kord päevas subkutaanselt
On ette nähtud alkaloidsoola lahus, mille moodustavad nõrk alus ja tugev hape. Stabilisaator (vesinikkloriidhappe lahus) on ette nähtud sõnadega. Lahuse pH väärtus peaks jääma vahemikku 3,5-4,5. Lahust steriliseeritakse voolava auruga 30 minutit.
22.5. Rp.: Solutionis Coffeini-natrii benzoatis 10% 50 ml
steriliseerimine!
D.S. 1 ml 2 korda päevas subkutaanselt
Määratakse aine lahus, mis on tugeva aluse ja nõrga happe sool. GPC suunas lisatakse stabilisaatorina 0,1 N. naatriumhüdroksiidi lahus kiirusega 4 ml 1 liitri lahuse kohta. Sel juhul lisage 0,2 ml naatriumhüdroksiidi lahust, pH 6,8-8,0. Lahust steriliseeritakse voolava auruga 30 minutit.
22.6. Rp.: Solutionis Acidi ascorbinici 5% 25 ml
steriliseerimine!
D.S. 1 ml 2 korda päevas intramuskulaarselt
Määratakse kergesti oksüdeeruva aine lahus. Stabiliseerimiseks valmistatakse lahus antioksüdandiga (naatriummetabisulfit 0,1% või naatriumsulfit 0,2%). Samal põhjusel kasutatakse värskelt keedetud ja süsihappegaasiga küllastunud vett. Tuleb meeles pidada, et askorbiinhappe lahused põhjustavad keskkonna tugevalt happelise reaktsiooni tõttu valuaisting. Söötme neutraliseerimiseks lisatakse stöhhiomeetrilise arvutuse kohaselt lahusesse naatriumvesinikkarbonaat. Saadud naatriumaskorbaat säilitab täielikult askorbiinhappe raviomadused. Ravimite valmistamisel juhinduvad nad tehnoloogiast ja arvutustest, mis on toodud GFH art. 7 „Solutio Acidi ascorbinici 5% pro injectionibus”. Steriliseerige voolava auruga 15 minutit.
22.7. Rp.: Solutionis Glucosi 40% 100 ml
steriliseerimine!
D.S. 20 ml 3 korda päevas intravenoosselt
Laialdaselt ja erinevates kontsentratsioonides (5 kuni 40%) ettenähtud glükoosilahustes kasutatakse stabilisaatorit, mis koosneb 0,26 g naatriumkloriidi ja 5 ml 0,1 N segust. vesinikkloriidhappe lahus 1 liitri glükoosilahuse kohta. Töö kiirendamiseks on soovitatav kasutada retsepti järgi saadud eelnevalt valmistatud stabilisaatorilahust: 5,2 g naatriumkloriidi, 4,4 ml lahjendatud soolhapet (täpselt 8,3%) ja destilleeritud vett kuni 1 liiter. Glükoosilahustele lisatakse stabilisaatorlahust koguses 5% (olenemata glükoosi kontsentratsioonist). Selles stabilisaatoris sisalduv vesinikkloriidhape, neutraliseerides klaasi leeliselisuse, vähendab glükoosi karamelliseerumise ohtu. Arvatakse, et naatriumkloriid moodustab aldehüüdrühma kinnituskohas kompleksseid ühendeid ja takistab seeläbi lahuses redoksprotsesse. Stabiliseeritud glükoosilahust steriliseeritakse voolava auruga 60 minutit või 119-121 ° C juures 8 minutit (mahuga kuni 100 ml). Glükoosilahused on hea kasvulava mikroorganismidele ja on tavaliselt nendega väga saastunud, mistõttu on vaja pikemat steriliseerimisperioodi. Kollakaid glükoosilahuseid tuleb loksutada väikese koguse lahusega aktiveeritud süsinik ja filtreerida. Glükoosi süstelahuste valmistamisel tuleb arvestada, et see sisaldab kristallisatsioonivett ja võib sisaldada hügroskoopset vett, mistõttu tuleks seda rohkem arvestada, kasutades GFH-s toodud arvutusvalemit (artikkel 311):
![]()
kus a on retseptis märgitud veevaba glükoosi kogus; b - vee protsent glükoosis vastavalt analüüsile. Meie puhul: a = 40 g; b = 10,5%; P = 44,7 g.
Glükoosi vesilahuse maht pärast lahustumist on 30,8 ml (FV = 0,69).
Stabilisaatori kogus (Weibeli lahus) - 5 ml. Vee kogus lahuse jaoks - 100 - (5 + 30,8) = 64,2 ml.
Lahuse tehnoloogia: aseptilistes tingimustes lahustatakse 44,7 g glükoosi steriilses statiivis 64,2 ml steriilses süstevees. Lahus filtreeritakse steriilsesse viaali, lisatakse 5 ml steriilset Weibeli lahust. Steriliseerige voolava auruga 60 minutit.
22.8. Rp.: Olei camphorati 20% 50 ml
steriliseerimine!
D.S. 2 ml subkutaanselt
Määrati õline süstelahus. Kamper lahustatakse enamikus soojas (40–45 °C) steriliseeritud virsiku (aprikoosi, mandli) õlis. Filtreeritakse läbi kuiva filtri kuiva mõõtekolbi ja lahjendatakse õliga märgini, loputades kaevufiltrit. Pärast seda viiakse kolvi sisu lihvimiskorgiga steriilsesse viaali. Valmis lahuse steriliseerimine viiakse läbi voolava auruga tund aega. Seda toimingut tuleb pidada garantiiks, kuna söötme saastest puhastamine on saavutatud juba õli steriliseerimise ajal.
Plasma asenduslahused. Plasmaasendajad on lahused, mis on ette nähtud plasma asendamiseks ägeda verekaotuse ja šoki korral erinevat päritolu, mikrotsirkulatsiooni häired, mürgistus ja muud hemodünaamiliste häiretega seotud protsessid. Neid nimetatakse vereasendajateks, kui sellised lahused sisaldavad vormitud elemendid veri (lisatakse verd). Plasma asendavad lahused jagunevad otstarbe ja funktsionaalsete omaduste järgi peamiselt rühmadesse: 1) lahused, mis reguleerivad vee-soola ja happe tasakaalu; 2) võõrutuslahused ja 3) hemodünaamilised lahused.
Suurem osa plasmat asendavatest lahustest on valmistatud tööstuslikes tingimustes dekstraani, polüvinüülpürrolidooni ja polüvinüülalkoholi ning muude makromolekulaarsete ühendite baasil. Mõned soolalahused valmistatakse siiski endiselt riigis apteegi tingimused, peamiselt raviasutusi teenindavates apteekides.
Isotooniline naatriumkloriidi lahus. Naatriumkloriidi sisaldus tagab suures osas vere osmootse rõhu (7,4 atm) püsivuse. Naatriumkloriidi olulise puuduse, silelihaste spasmide, talitlushäiretega närvisüsteem ning vereringet ja vere paksenemist täheldatakse vee ülemineku tõttu veresoonte voodist kudedesse. Naatriumkloriidi vesilahusel, mis sisaldab 0,9% seda ainet, on sama osmootne rõhk kui verel ja seetõttu on selle lahus näidatud kontsentratsioonil inimese vereplasma suhtes isotooniline. Isotoonilist naatriumkloriidi lahust nimetatakse sageli "füsioloogiliseks", mis on vale, kuna see ei sisalda peale Na + ja Cl- muid ioone, mis on vajalikud kehakudede füsioloogilise seisundi säilitamiseks. Isotoonilise naatriumkloriidi lahuse peamine kasutusala on keha dehüdratsiooni ja mürgistuse korral. mitmesugused haigused(äge düsenteeria, toidumürgitus jne).
Isotoonilist naatriumkloriidi lahust kasutatakse sageli lahustina isotoniseerimist vajavate ravimainete süstelahuste jaoks.
22.9. Rp.: Solutionis Natrii chloridi
isotonicae pro injectionibus 100 ml
D.S. Manustada tilguti intravenoosselt
Lahus on valmistatud kõrge puhtusastmega naatriumkloriidist (keemiliselt puhas või analüütiliselt puhas), mis on eelnevalt steriliseeritud kuiva kuumusega temperatuuril 180 °C 2 tundi pürogeenivabas vees. Väikesed kogused (100, 200 ml) lahust valmistatakse mugavalt spetsiaalsetest 0,9 g naatriumkloriidi tablettidest (proovi võetud tabletid). Steriliseerige 1,19-1,21°C juures 15-20 minutit.
Füsioloogiline Ringer-Locke lahus. See lahus valmistatakse järgmise retsepti järgi:
Naatriumkloriid 9,0
Naatriumvesinikkarbonaat 0,2
Kaaliumkloriid 0,2
Kaltsiumkloriid 0,2
Glükoos 1.0
Süstevesi kuni 1000 ml
Ringer-Locke'i lahus on rikastatud K + ja Ca ++ ioonidega, sisaldab süsinikdioksiidi, samuti energiaallikat - glükoosi. Süsinikdioksiid, sisenedes verre, ergastab hingamis- ja vasomotoorseid keskusi. Selle lahuse valmistamise eripäraks on naatriumvesinikkarbonaadi steriilse lahuse ja ülejäänud koostisosade steriilse lahuse eraldi valmistamine. Enne patsiendile manustamist lahused kurnatakse. Lahuste eraldi valmistamine takistab kaltsiumkarbonaadi sademe teket. Naatriumvesinikkarbonaadi lahuste valmistamist on kirjeldatud eespool. Selle valmistamiseks võite võtta 500 ml pürogeenivaba vett, ülejäänud 500 ml vees lahustatakse naatriumkloriid, glükoos ning kaalium- ja kaltsiumkloriid (viimane võetakse kontsentraadi kujul tilkhaaval). Valmistatud lahused steriliseeritakse voolava auruga.
Süstitavate ravimvormide vabastamine. Veahoiatus
Süstelahuste koostisesse kuuluvad mürgised ained kaalub kontrolör apteekri juuresolekul, kes peab veenduma, et aine mass on õige ja sobiv, ning edastab talle koheseks lahuse valmistamiseks.
Pärast korkimist seotakse steriliseerimiseks valmistatud lahustega viaalid küpsetuspaberiga, millele apteeker peab tegema musta grafiitpliiatsiga (mitte tindiga) pealdise saabuvate koostisosade ja nende kontsentratsiooni kohta ning isiklikult allkirjastama. Võimalikud on ka muud tüüpi märgised (näiteks metallist märgid). Pärast steriliseerimist kleebib apteeker lahustega pudelitele numbri, meditsiiniasutuste apteekides - sildid ja edastab need koos retseptiga tehnoloog-apteekrile kontrollimiseks ja järgnevaks registreerimiseks.
Kõiki süstelahuseid enne ja pärast steriliseerimist tuleb kontrollida mehaaniliste lisandite puudumise suhtes ja läbida täielik keemiline kontroll, sealhulgas identifitseerimine, raviainete kvantitatiivne sisaldus, söötme pH, isotoonilised ja stabiliseerivad (ainult enne steriliseerimist) ained. Individuaalsete retseptide või raviasutuste nõuete järgi valmistatud süstelahuseid kontrollitakse keemiliselt valikuliselt ettenähtud korras.
Kontroll apteekri küsitlemise teel viiakse läbi kohe pärast süstelahuste valmistamist. Lisaks monitooringulahendustele peab tehnoloog-apteeker kontrollima steriliseerimise teostamise temperatuuri ja selle kestust, arvestades steriliseeritava aine omadusi. Valmistatud süstelahuse vabastamiseks koostab tehnoloog-apteeker pärast retsepti, allkirja ja viaali pealdiste võrdlemist.
Süstelahuste jaoks kõige laialdasemalt kasutatavad lahustid on süstevesi.- Aqua pro injekcijibus - ja taimeõlid. Tavaline destilleeritud vesi ei sobi süstelahuste valmistamiseks, kuna see võib sisaldada pürogeenseid aineid. Vee steriliseerimine põhjustab ainult mikroorganismide surma, hukkunud mikroobid, jääkained ja mikroorganismide lagunemine jäävad vette ning omavad pürogeenseid omadusi, põhjustavad teravat külmavärinat ja suurtes kogustes isegi. surmav tulemus. Koos
Ülejäänud pürogeensetest ainetest pole siiani hästi aru saadud. Arvatakse, et need kuuluvad kompleksühenditesse nagu kompleksvalgud, polüsahhariidid, lipopolüsahhariidid, mõned pürogeensed ained sisaldavad kuni 75% fosforit sisaldavaid polüsahhariide ja kuni 25% rasvataolisi aineid. Arvatakse, et pürogeenne toime tuleneb fosfaatrühmade olemasolust.
Pürogeensed reaktsioonid ilmnevad kõige enam intravaskulaarsete, spinaalsete ja intrakraniaalsete süstidega. Sellega seoses tuleks süstelahuseid valmistada veest, mis ei sisalda pürogeenseid aineid. Pürogeensed ained ei ole lenduvad ega destilleeru koos veeauruga. Nende sattumine destillaati on seletatav väikseimate veepiiskade kaasahaaramisega aurujoaga külmikusse.
Seetõttu on pürogeenivaba vee saamisel põhiülesanne veeauru puhastamine tilkuvast vesifaasist. Selleks kasutatakse praegu laialdaselt aparaati AA-1 (aparaat pürogeenivaba vee saamiseks).
Selles seadmes kraanivesi lisatakse keemilisi reaktiive (kaaliumpermanganaat - orgaaniliste ainete oksüdeerimiseks, kaaliummaarjas - ammoniaagi püüdmiseks ja muutmiseks mittelenduvaks ammooniumsulfaadiks ja dinaatriumfosfaadiks - vesinikkloriidhappe muundamiseks mittelenduvaks naatriumkloriidiks). Saadud segu destilleeritakse. Püüniste läbiv aur puhastatakse tilkfaasist, siseneb kondensatsioonikambrisse, jahutatakse väljastpoolt külma veega ja kondenseerumisel muutub pürogeenivabaks veeks.
Süstevesi peab vastama kõigile destilleeritud vee nõuetele ja olema pürogeenivaba. Sobib kasutamiseks kuni 24 tundi, kui seda hoitakse aseptilistes tingimustes. Sanitaar-epidemioloogiajaamad on kohustatud kord kvartalis teostama selektiivset süstevee ja pürogeensete ainete puudumise bakterioloogilist kontrolli.
"Apteekide apteekri käsiraamat", D.N. Sinev
Tootmisprotsess koosneb järgmistest etappidest:
1. Ettevalmistav, sh: arvutuste tegemine, aseptilise tootmise tingimuste koostamine, anumate ja pakendite pesemine ja steriliseerimine, süstevee hankimine.
2. Süstelahuste hankimine, sealhulgas toimingud: lahustamine, filtreerimine, villimine, korkimine, puudumise kontrollimine
mehaaniliste lisandite kontroll, täielik keemiline analüüs, steriliseerimine.
3. Valmistoodete märgistamine.
Süstelahuste valmistamise tüüpiline tehnoloogiline skeem on näidatud skeemil 5.1. Tootmisprotsess on jagatud 3 voogu:
Mahutite ja pakendite ettevalmistamine;
Lahuse valmistamine;
Valmistoodete steriliseerimine, kvaliteedikontroll, pakendamine ja märgistamine.
Süste- ja infusioonilahuste saamiseks kasutatakse neutraalseid klaaspudeleid kaubamärgiga HC-1 (ravimid, antibiootikumid) ja HC-2 (veresooned). Erandina (pärast leelisusest vabanemist) kasutatakse AB-1 ja MTO klaasist valmistatud viaale. Nendes olevate lahuste kõlblikkusaeg ei tohiks ületada 2 päeva.
Töötlemise ajal täidetakse leeliselised klaaspudelid puhastatud veega, steriliseeritakse temperatuuril 120 ° C 30 minutit. Pärast töötlemist jälgitakse selle efektiivsust (potentsiomeetrilise või acidimeetrilise meetodiga). Vee pH väärtuse muutus enne ja pärast viaalis steriliseerimist ei tohiks olla suurem kui 1,7.
Uusi nõusid pestakse seest ja väljast kraaniveega, leotatakse 20–25 minutit temperatuurini 50–60 °C kuumutatud pesulahustes. Kasutatakse ka sinepi suspensiooni 1:20, 0,25% Desmoli lahust, 0,5% Progressi, Lotuse, Astra lahuseid, 1% SPMS-i lahust (sulfanooli segu naatriumtripolüfosfaadiga 1:10). Tugeva saastumise korral leotatakse nõusid 2-3 tundi 5% sinepisuspensioonis või -lahuses. pesuvahendid vastavalt erijuhistele.
Pestud nõud steriliseeritakse kuuma õhuga temperatuuril 180 ° C 60 minutit. Kasutatud nõud desinfitseeritakse: 1% aktiveeritud klooramiini lahus - 30 minutit; 3% värskelt valmistatud vesinikperoksiidi lahus, millele on lisatud 0,5% pesuainet - 80 minutit või 0,5% Dezmol lahus - 80 minutit.
Süstelahustega viaalide sulgemiseks kasutatakse spetsiaalset kummist korke: IR-21 (silikoon); 25 P (looduslik kumm); 52-369, 52-369/1, 52-369/P (butüülkummi); IR-119, IR-119A (butüülkummi). Uued kummikorgid
Skeem 5.1. Tüüpiline tehnoloogiline skeem lahenduste valmistamiseks
töödeldud väävli, tsingi ja muude ainete eemaldamiseks nende pinnalt vastavalt juhistele.
Kasutatud korgid pestakse puhastatud veega ja keedetakse selles 2 korda 20 minutit, steriliseeritakse temperatuuril 121 + 2 ° C 45 minutit.
Lahuste valmistamisel kasutatakse süstevett (vt ptk 21) ja kvalifikatsiooniga "Süstimiseks" või muid ravimeid, kui vastavas API-s on märgitud.
Süstelahuste filtreerimine toimub läbi sügavate, sageli membraanfiltrite (vt peatükki "Asepsis, steriliseerimine filtreerimise teel").
Väikeste koguste süstelahuste valmistamisel kasutatakse filtrit "Fungus" (joon. 25.13), mis on filtermaterjaliga kaetud ja vaakumis töötav lehter. Filterkott koosneb 2 kihist siidiriidest, 3 kihist filterpaberist, marlipadjast ja 2 kihist siidiriidest. Täielikult täidetud lehter seotakse peale langevarjusiidiga. Filtreeritakse vaakumis.
Filtreeritud lahus valatakse dosaatorite abil süstelahuste jaoks ettevalmistatud pudelitesse. Sulgege korkidega.
Kummist korgiga suletud süstelahustega viaalid on kontrollitud mehaaniliste lisandite puudumise suhtes. Kui lahuse esmasel kontrollimisel tuvastatakse mehaanilisi lisandeid, siis see filtreeritakse.

Riis. 5.13. Seenefilter:
1 - lehter, kaetud filtrimaterjalide kihiga; 2 - lahenduse toiteliin; 3 - klaas filtreeritud lahusega; 4 - vaakum; 5 - filtreeritud lahusega vastuvõtja; 6 - lõks vaakumtorule
Pärast valmistamist tehakse süstelahuste keemiline analüüs, mis seisneb ravimvormi moodustavate ravimainete autentsuse (kvalitatiivne analüüs) ja kvantitatiivse sisalduse määramises (kvantitatiivne analüüs). Kvantitatiivseid ja kvalitatiivseid analüüse viivad läbi eelkõige apteekrid-analüütikud kõikidele süstelahuste seeriatele, mis valmistatakse apteegis (enne steriliseerimist). Apteekides, kus apteekrit-analüütikut pole, analüüsitakse kvantitatiivselt atropiinsulfaadi, novokaiini, glükoosi, kaltsiumkloriidi ja isotoonilise naatriumkloriidi lahuse lahuseid. Kontroll apteekri-tehnoloogi küsitlemisega toimub kohe pärast süstelahuse valmistamist. Kell positiivne tulemus kaetud metallkorkidega.
Süstelahuste tootmise tehnoloogilises protsessis on 6 peamist etappi:
Ettevalmistustööd
Lahenduse tegemine
Filtreerimine ja pakendamine
Lahuse steriliseerimine
Valmistoodete kvaliteedikontroll
Puhkuse korraldus
Erilist tähelepanu tuleks pöörata asjaolule, et vastavalt Vene Föderatsiooni tervishoiuministeeriumi korraldusele nr. steriilsete lahuste valmistamine on keelatud, kui puuduvad andmed neis sisalduvate ravimainete keemilise sobivuse, steriliseerimise tehnoloogia ja viisi kohta, samuti täieliku keemilise kontrolli analüüsimeetodite puudumisel.
Ettevalmistustööd hõlmavad ruumide, seadmete, õhu desinfitseerimise, nõude, sulgurite, abimaterjalide, lahusti, raviainete, aga ka personali ettevalmistamist. Need meetmed on reguleeritud Vene Föderatsiooni tervishoiuministeeriumi 21. oktoobri 1997. aasta korraldusega nr 309. Ennetusmeetmete loetelu on toodud ka kvaliteedikontrolli juhendi punktis 3 ravimid toodetud apteekides, mille on heaks kiitnud Vene Föderatsiooni tervishoiuministeerium 16. juunil 1997. aastal. tellimuse number 214.
1) Aseptikaüksuse ruumide ja sisseseade nõuded ja ettevalmistus tööks.
Süstelahuste valmistamine toimub aseptilises üksuses. Aseptilise üksuse ruumid peaksid asuma isoleeritud sektsioonis ja välistama "puhta" ja "määrdunud" õhuvoolu ristumiskoha. Aseptiline plokk peab olema eraldi sissepääsuga või eraldatud teistest tootmisruumidest väravatega.
Enne aseptikasse sisenemist tuleb asetada kummimatid või poorsest materjalist matid, mis on niisutatud desinfitseerimisvahenditega (0,75% kloramiini B lahus 0,5% pesuainega või 3% vesinikperoksiidi lahus 0,5% pesuainega).
Lukk peaks olema varustatud spetsiaalsete lahtritega vahetusjalatsite pingiga. jalatsid, riidekapp hommikumantli ja bixi jaoks koos steriilsete riiete komplektidega, kraanikauss (küünar- või jalaajamiga segisti), elektriline õhukuivati ja peegel, hügieeniline kätehoolduskomplekt, riiete vahetamise ja kätehoolduse juhised , käitumisreeglid aseptilises üksuses.
Assistent-aseptikas ei ole veevarustus ja kanalisatsioon lubatud.
Seinte kaitsmiseks kahjustuste eest materjalide või toodete (kärud jne) transportimisel on vaja ette näha spetsiaalsed nurgad või muud seadmed.
Vältimaks õhu sattumist koridori ja tööstusruumidesse aseptikasse, on vaja viimases tagada sissepuhke- ja väljatõmbeventilatsioon. Sel juhul tuleks õhuvoolude liikumine suunata aseptilisest seadmest külgnevatesse ruumidesse, kusjuures sissevool domineerib heitgaasist.
Soovitatav on kasutada spetsiaalseid seadmeid puhta õhu horisontaalsete või vertikaalsete laminaarsete voogude tekitamiseks kogu ruumis või eraldi lokaalsetes piirkondades, et kaitsta kõige kriitilisemad alad või toiminguid (puhtad kambrid) või laminaarse õhuvooluga laudu. Neil peavad olema siledast vastupidavast materjalist tööpinnad ja kork.
Laminaarne voolukiirus jääb vahemikku 0,3-0,6 ms? No regulaarsel steriilsuse kontrollil vähemalt kord kuus.
Aseptilises üksuses on vaja säilitada laitmatu puhtus. Assistendi märgpuhastus - aseptiline ruum viiakse läbi vähemalt üks kord vahetuses vahetuse lõpus, kasutades desinfitseerimisvahendeid. Mitte mingil juhul ei tohi keemilist puhastust lubada. Kord nädalas tehakse üldpuhastus, võimalusel koos tehnika vabastamisega.
Aseptilise ploki puhastamisel on vaja rangelt järgida etappide järjestust. Alustada tuleks aseptikast. Esmalt peske seinad ja uksed laest põrandani. Liigutused peaksid olema sujuvad, alati ülevalt alla. Seejärel pesevad ja desinfitseerivad statsionaarseid seadmeid ja kõige lõpuks põrandaid.
Kõik aseptikasse toodud seadmed ja mööbel on eelnevalt töödeldud desinfitseerimislahusega.
Desinfitseerimislahuste peab valmistama spetsiaalselt koolitatud personal vastavalt kehtivatele juhistele.
Kõvade pindade, seinte ja põrandate desinfitseerimiseks võib kasutada järgmisi desinfitseerimisvahendeid.
Tabel 2.1
Tootmisjäätmed ja prügi tuleb koguda spetsiaalsetesse ajamikaanega konteineritesse. Prügi tuleb ära viia vähemalt üks kord vahetuses. Käsipesukausse ja prügikaste puhastatakse ja desinfitseeritakse iga päev.
2) Õhu desinfitseerimine.
Õhu ja erinevate pindade desinfitseerimiseks aseptilises ruumis paigaldatakse avatud või varjestatud lampidega bakteritsiidsed emitterid (statsionaarsed või mobiilsed). Bakteritsiidsete lampide arv ja võimsus tuleks valida vähemalt 2-2,5 W varjestamata emitteri võimsuse alusel 1 m3 ruumi mahu kohta. Varjestatud bakteritsiidsete lampidega - 1 W 1 m² kohta.
Seinale paigaldatavad bakteritsiidsed kiiritajad OBN-150 paigaldatakse kiirusega 1 kiiritaja 30 m² ruumi kohta; lakke paigaldatav OBP-300 - kiirusega üks 60 m² kohta; avatud lampidega mobiilset OBP-450 kasutatakse õhu kiireks desinfitseerimiseks kuni 100 m3 ruumides. Optimaalset efekti täheldatakse 5 m kaugusel kiiritatud objektist.
Avatud bakteritsiidseid lampe kasutatakse inimeste puudumisel töövaheaegadel, öösel või spetsiaalselt selleks ettenähtud ajal enne tööd 1-2 tundi. Avatud lampide lülitid peaksid asuma tootmisruumi sissepääsu ees ja olema varustatud signaalsildiga "Bakteritsiidsed lambid põlevad" või "Ärge sisenege, bakteritsiidne kiiritaja on sisse lülitatud".
Keelatud on viibida ruumides, kus kasutatakse varjestamata lampe. Ruumi sisenemine on lubatud alles pärast varjestamata bakteritsiidse lambi väljalülitamist ja pikaajaline viibimine määratud ruumis on lubatud ainult 15 minutit pärast selle väljalülitamist.
Varjestatud lampide kasutamisel võib õhu desinfitseerimist läbi viia inimeste juuresolekul. Nendel juhtudel asetatakse lambid spetsiaalsetesse liitmikesse põrandast vähemalt 2 m kõrgusele. Liitmikud peaksid suunama lambi kiired horisontaalpinnast ülespoole 5–80º nurga all.
Varjestatud bakteritsiidlambid võivad töötada kuni 8 tundi päevas. Kui pärast 1,5-2 tundi lampide pidevat töötamist on piisava ventilatsiooni puudumisel õhus tunda osoonilõhna, on soovitatav lambid 30-60 minutiks välja lülitada.
Statiivi kiiritusseadme kasutamisel mis tahes pindade spetsiaalseks kiiritamiseks tuleb see viia võimalikult lähedale, et kiiritada vähemalt 15 minutit.
3) Personali koolitus.
Inimesed kannavad ja viivad keskkonda palju baktereid, viirusi, hallitusseente, eoseid, kiude, mis lahusega kokku puutudes võivad muuta selle kasutamise ohtlikuks.
Operatsiooniruumis, st kui seal on personal, suureneb osakeste ja mikroorganismidega saastumine järsult. Nõutava puhtuse taseme säilitamiseks kasutatakse spetsiaalset riietust, mis vähendab saastumise taset, kuna aeglustab väikeste osakeste tungimist väljapoole. Lisameetmed hõlmavad peakatte kandmist ja korralikku kätepesu. Suhteliselt väikeste liigutustega paiskab inimene keskkonda 500 tuhat kuni 4 miljonit osakest. Kuni 10% osakestest võib sisaldada mikroorganisme.
Väljapaisatavate osakeste arv sõltub inimese aktiivsusest ja riietuse tüübist. Osakeste arvu on võimalik vähendada 10 või 100 korda läbi sobiva riietuse ja käitumise aseptilises üksuses.
Aseptilises osakonnas töötamiseks peab teil olema spetsiaalne hügieeniriietuse komplekt: hommikumantel või pükskostüüm või kombinesoon (krae-statiiv on optimaalne, vöökohalt seotud, kätised on liibuvad); spetsiaalsed kingad ja jalatsikatted; mütsid või suud ja nina katva maskiga kiiver või kapuuts, vajadusel kummikindad ilma talgita. Komplekt peab olema valmistatud materjalist või segatud kangas mis vastavad hügieeninõuetele, minimaalse ebemega.
Riidekomplekti steriliseeritakse jalgratastes aurusterilaatorites 120 °C juures 45 minutit või 132 °C juures 20 minutit, kinnistes jalgratastes mitte üle 3 päeva. Võimalusel kasutage ühekordselt kasutatavaid steriilseid riideid.
Töötajate jalanõud desinfitseeritakse enne ja pärast tööd ning hoitakse õhuluku suletud kappides või sahtlites. Desinfitseerimiseks pühkige väljast kaks korda 1% või 0,75% kloramiin B lahusega, millele on lisatud 0,5% pesuainet, või 3% vesinikperoksiidi lahusega, millele on lisatud 0,5% pesuainet. Lisaks tehakse jalatsite desinfitseerimine 40% formaldehüüdi või 40% äädikhappe lahusega niisutatud vatikotis, mis on neutraliseeritud ammoniaagi või naatriumhüdroksiidi lahusega.
Aseptilisse ruumi sisenemine ja sealt väljumine, vajalike materjalide ja esemete transportimine peab toimuma läbi õhuluku. Iga aseptilise ruumi sissepääsu juures tuleks vahetada steriilsete riiete komplekt.
Väravast sisenedes pannakse jalga spetsiaalsed jalanõud. Soovitav on varustada alumisse ossa kahepoolne pink jalatsite jaoks. Pingil istudes võtab töötaja sussid jalast ja asetab need eraldi kambrisse. Seejärel, heites jalad üle pingi, pöörab ta 180º ja võtab üksikult riiulilt või riiulilt steriilsete tehniliste riietega paki või biksi. Pink on ette nähtud ettevalmistamise etappide tinglikult eraldamiseks. Pärast käte pesemist ja kuivatamist pange selga steriilsed riided, välja arvatud kindad, seejärel ravige käsi ja vajadusel kandke kätte steriilsed kindad.
Käte naha desinfitseerimiseks 70% etüülalkoholi või muid alkoholi sisaldavaid preparaate (AKhD-2000, oktoniderm, oktonisept), kloorheksidiini biglukonaadi 0,5% lahust (70% etüülalkohol), jodopürooni ja teiste jodofooride (jodonaat, jodovidoon) lahus 1%, kloramiin B lahus 0,5% (teiste ravimite puudumisel) või muu Vene Föderatsiooni tervishoiuministeeriumi poolt selleks otstarbeks lubatud vahend.
Käte desinfitseerimisel alkoholi sisaldavate preparaatidega pühitakse need lahuses niisutatud marlilapiga, saavutades naha pruunistumise. Kloorheksidiini ja jodofooride lahuste kasutamisel kantakse ravimit peopesadele koguses 5-8 ml ja hõõrutakse käte nahka. Käte töötlemisel klooramiini B lahusega kastetakse need lahusesse ja pestakse 2 minutit ning seejärel lastakse kätel kuivada.
Töötamise ajal peaks aseptilises üksuses olema minimaalne nõutav arv töötajaid. Personali liikumine peaks olema aeglane, sujuv, ratsionaalne. Vältige äkilisi liigutusi, piirake vestlusi ja liigutusi. Kui on vaja töötajatega verbaalselt suhelda väljaspool aseptilist üksust, tuleks kasutada telefoni või muud sisetelefoni.
Märkmete jaoks tuleks kasutada eelnevalt lõigatud pärgamendilehti ja pastapliiatseid või viltpliiatseid, mida tuleks desinfitseerimisvahenditega niisutatud ebemevaba lapiga üle pühkida.
Aseptilistes tingimustes töötades on keelatud:
- - siseneda aseptikaruumi mittesteriilsetes riietes ja lahkuda aseptikast steriilsetes riietes;
- - omama steriilse hügieeniriietuse all mahukaid fliisi riideid või riideid, milles töötaja viibis tänaval;
- - kasutada kosmeetikat või aerosooldeodorante;
- - kanda kellasid või ehteid;
- - tuua sisse isiklikud asjad (võtmed, kammid, taskurätikud jne);
- - puhastage nina. Selleks tuleks minna õhulukku, kasutada steriilset taskurätikut ja salvrätikuid, seejärel käsi pesta ja desinfitseerida;
- - korjata üles ja taaskasutada põrandale kukkunud esemeid;
- - hõõruge käsi või nägu, kratsige pead, kummarduge ravimainetega pudelite või muude anumate kohale;
- - kasutage pliiatseid, täitesulepead, kustutuskummid.
- 4) Nõude ja sulgurite valmistamine.
Klaasmahuteid kasutatakse ravimitööstuses enim ravimite hoidmiseks ja transportimiseks, samuti ravimite otse haiglasse väljastamiseks.
Ravimite kvaliteeti mõjutavad ka klaasi tüüp ja omadused.
Klaasi omadused sõltuvad selle koostisosadest ja nende vahekorrast sulamis. Klaasi kõige olulisem kvaliteet on selle keemiline vastupidavus.
Keemilist vastupidavust iseloomustab klaasi vastupidavus agressiivse keskkonna hävitavale toimele.
Seega võib klaaspaketi sees oleva keskkonna pH tõus põhjustada ravimainete farmatseutilise aktiivsuse kadumise. Eriti oluline on nende klaasi omadustega arvestada, kui hoiustate väikestes annustes väga aktiivseid raviaineid, mis leeliselises keskkonnas kergesti inaktiveeruvad (vitamiinid, antibiootikumid, glükosiidid). Lisaks võib leeliselises keskkonnas toimuda orgaaniliste aluste eraldamise protsess nende sooladest, samuti kiireneb oluliselt fenoolhüdroksiidide oksüdatsiooniprotsess. Leeliseline klaas võib samuti soodustada mikrofloora arengut.
Klaasi leostumise protsessi saab ära hoida või minimeerida nõude eritöötlusega, spetsiaalsete klaaside kasutamisega, samuti lisades ravimlahusele vastuvõetavates kogustes mineraalhappeid, mis neutraliseerivad tekkiva leeliselise lisandi.
Klaasi kaubamärgid on märgitud eraartiklites. Anumad peavad olema valmistatud materjalidest, mis ei takista sisu visuaalset kontrollimist ning korkmaterjal peab olema tugev ja elastne.
Süstelahused valatakse ja väljastatakse neutraalsetesse klaasviaalidesse (NS), vereviaalidesse, kaubamärgi NS-2 või NS-2l klaasist vastavalt GOST H)-782-85, suletakse kummikorgiga ja keeratakse või rullitakse. korgid või viaalides drota ravimite (antibiootikumide) jaoks kaubamärgi NS-1 klaasist.
Tuleb meeles pidada, et nüüd on tööstus lõpetanud neutraalklaasi kaubamärgiga farmaatsiaklaasi tootmise ja toodab MTO-klaasi (meditsiinipakendeid).
Vee võime lahustada klaasi üksikuid koostisosi avaldub juba esimestel minutitel lahuse kokkupuutel klaasiga, isegi toatemperatuuril, ning paraneb säilitamise ajal. Steriliseerimine mõjutab tugevalt lahuste pH-d ja seega ka nende stabiilsust ning mõjutab keha.
Kui klaasnõud jõuavad apteeki ilma klaasi marki täpsustamata, on vaja määrata klaasi aluselisus.
Lisaks uutele lauanõudele saab apteeki ka kasutatud nõud ehk nn tagastatav pakend.
Ravimilahused puutuvad vahetult kokku pudeli või viaali klaasi sisepinnaga nii steriliseerimise ajal kui ka sobivates säilitustingimustes või kasutamise ajal. Seetõttu dikteerivad steriilsete lahuste puhtuse nõuded kasutatava pakendi kvaliteedi nõuded. Viaalide ja pudelite töötlemise tehnikad hõlmavad selliseid meetodeid nagu desinfitseerimine, pesemine (pesu-desinfitseeriv töötlemine), loputamine ja steriliseerimine, samuti klaasnõude töötlemise kvaliteedikontroll.
Desinfitseerimiseks kasutage 1% aktiivse klooramiini lahust nõude kastmisega 30 minuti jooksul või vesinikperoksiidi 3% lahust 80 minuti jooksul.
Vene Föderatsiooni tervishoiuministeeriumi ja TIN apteegi 2. märtsi 1998. aasta kirjaga. nr 20-8/38 väärikuse juhendis nõude desinfitseerimise vahendite loetelu. apteegi režiimi (tellimus nr 309) täiendati desinfektsioonivahenditega Klorcept ja Klor-Klint.
Desinfitseerimislahuste valmistamine toimub spetsiaalselt koolitatud personali poolt. Valmistatud desinfektsioonivahendite lahuste säilitamine ei tohiks ületada 24 tundi. Sama lahuse korduvkasutamine ei ole lubatud.
Pesemine toimub nõusid leotades sobiva kontsentratsiooniga pesuaine lahuses, mis on kuumutatud temperatuurini 50-60 ° C. Nõusid leotatakse 25-30 minutit täielikult sukeldades. Tugevalt määrdunud nõusid leotatakse pikemat aega. Samas lahuses pestakse nõusid ruffiga. Sinepiga pesemisel viiakse läbi hõõrumine kuum vesi, ja sünteetiliste pesuvahendite kasutamisel on võimalik pesumasinaga pesemine ja loputamine.
Tagastatud nõusid on kõige ratsionaalsem töödelda pesu- ja desinfektsioonivahendite lahusega. Sel eesmärgil on tugevalt määrdunud nõude puhul soovitatav kasutada 1% kloramiini lahust või 0,2% DP-2 lahust 120-minutilise sukeldamisega. Ülejäänud nõude puhul kasutage 0,5% kloori lahust, 0,2% DP-2 lahust või 3% vesinikperoksiidi lahust, millele on lisatud 0,5% pesuainet. Sel juhul kastetakse nõud 15 minutiks täielikult sooja lahusesse ja pestakse seejärel harjaga samas lahuses. Pärast seda pestakse neid jooksva kraaniveega (kuuma), kuni desinfektsioonivahendi lõhn täielikult kaob.
Loputage kraaniveega 5 korda, puhastatud - 3. Optimaalselt viiakse viimane loputus läbi süsteveega, filtreeritakse läbi filtri, mille pooride läbimõõt on 5 mikronit.
Nõusid steriliseeritakse kuuma õhuga - temperatuuril 180 ° C - 60 minutit või küllastunud auruga rõhu all temperatuuril 120 ° C - 45 minutit. Pärast temperatuuri langetamist sterilisaatoris 60-70 ° -ni suletakse nõud steriilsete korkidega.
Pestud nõude puhtust jälgitakse visuaalselt lisandite, plekkide, plekkide puudumise ning viaalide seintelt pärast nende loputamist voolava vee ühtluse järgi.
Kui on vaja tuvastada võimalikke rasvaseid saasteaineid nõude pinnal, tehakse tõrje Sudan 111 sisaldava reagendiga. Sünteetiliste pesuvahendite ja detergentide-desinfitseerimisvahendite loputamise täielikkus määratakse pH väärtusega potentsiomeetriliselt. Esialgu saab pesuaine jääkide olemasolu määrata fenoolftaleiiniga roosa värvimise teel.
Lisateavet kasutatud apteegiriistade töötlemise kohta leiate Vene Föderatsiooni tervishoiuministeeriumi 21. oktoobri 1997. aasta korraldusest nr 309. Lisaks tellimusele lisaks 1999.a. Farmaatsia Teadusliku Instituudi ravimitehnoloogia labor töötas välja 12. detsembril 1999 Tervishoiuministeeriumis kinnitatud juhendi (MÜ) nr 99/144 “Apteegis valmistatud steriilsete lahuste tehnoloogias kasutatavate nõude ja pesuvahendite töötlemine”. MU on välja töötatud normatiivdokumentatsiooni, oma eksperimentaaluuringute ja Desinfektoloogia Uurimise Instituudi eksperthinnangu alusel.
Süstelahuste tihendamiseks kasutatakse kummikorke.
Vene Föderatsiooni tervishoiuministeeriumi kiri 31. märtsist 1997 nr. Kasutamiseks soovitatav nr 29-3/143 on klorobutüülkummist sinine kork 53-599/3, millel on parim farmatseutiliste ja meditsiiniliste omaduste kompleks ning mis on kõige perspektiivsem pika säilivusajaga süste- ja infusioonilahuste korgiks. .
Kõrge toksilisuse tõttu on kork 25P (punane) süste- ja infusioonilahuste korkimisel keelatud.
Kõikide kaubamärkide kummist torkega korgid ei ole lubatud korduvkasutada, kuna üsna lai valik kummikorke suudab rahuldada tervishoiuasutuste vajadused nende järele.
Kuni 3-kuulise säilivusajaga süste- ja infusioonilahuste sulgemiseks korgid 52-599/1 (hall), 52-599/3 (sinine), 52-369/1 (must) ja I-51-2. kasutada (hall).
Tihenduslahuste puhul, mille säilivusaeg on üle 3 kuu, võib kasutada korke 52-599/1, 52-599/3 ja 52-396/1. Enne steriilsete lahuste sulgemist tuleb korgid töödelda. Töötlemismeetod on järgmine: pestakse käsitsi või pesumasinas 0,2% pesuaine lahuses nagu "Astra", "Lotus" temperatuuril 40-50 ° C 3 minutit, loputades 5 korda kuumaga. kraanivesi ja 1 kord puhastatud veega, keetmine trinaatriumfosfaadi 1% lahuses 30 minutit, pestes üks kord kraaniveega ja üks kord puhastatud veega, autoklaavides puhastatud vees temperatuuril 120 °C 60 minutit, pestes puhastatud vesi, auruga steriliseerimine biksides 120 °C juures 45 min. Steriilseid korke säilitatakse kinnistes jalgratastes mitte kauem kui 3 päeva, peale rataste avamist tuleks korgid ära kasutada 24 tunni jooksul.
Pärast vees autoklaavimist jalgrataste kotti korkide koristamisel ärge steriliseerige, kuivatage õhusterilisaatoris temperatuuril kuni 50 ° C 2 tundi ja hoidke jalgratastes või purkides jahedas kohas mitte rohkem kui 1 tund.
Korgid steriliseeritakse enne kasutamist nagu ülalpool. Siniste korkide 52-599/3 puhul võib autoklaavimise asemel kasutada 30-60 minutit puhastatud vees keetmist.
Sulgemismaterjali töötlemise ja ladustamise eeskirjad on märgitud ka Vene Föderatsiooni Tervishoiuministeeriumi 21. oktoobri 1997. a korralduse nr 309 juhendi 9. lisas.
Kummist korgiga suletud süstelahustega viaalid on rullitud metallkorgiga. Alumiiniumkorke hoitakse 15 minutit tellimuse nr 309 juhendis nimetatud 1-2% pesuainete lahuses, kuumutatakse temperatuurini 70-80 °C, seejärel lahus kurnatakse ja korgid pestakse voolava veega.
Puhtad korgid kuivatatakse jalgratastes õhusterilisaatoris temperatuuril 50–60 ° C ja hoitakse suletud anumates (jalgrattad, purgid, kastid) tingimustes, mis välistavad nende saastumise.
5) Tugimaterjali ettevalmistamine.
Abimaterjal pannakse ratastesse steriliseerimiseks kasutusvalmis kujul (lõigatud pärgament ja filterpaber, soovitud suurusega tükkideks lõigatud marli, tampoonide sisse rullitud vatt jne). Steriliseerige auru sterilisaatoris 120°C juures 45 minutit. Säilitatakse suletud anumates 3 päeva, peale avamist kasutatakse materjal ära 24 tunni jooksul.
Klaasnõud, mördid, portselantooted steriliseeritakse küllastunud auruga ülerõhul 132 ° C - 20 minutit või õhusterilisaatoris temperatuuril 180 ° C - 60 minutit. Steriliseerimiseks kasutatakse pakendeid, mis on valmistatud pärgamentpaberist, topeltvooderdatud kalikonist või avatud anumates (bixid, karbid).
6) Lahusti valmistamine ja valik
Süstelahuste valmistamiseks kasutatavad ravimained ja lahustid peavad vastama GF, FS või VFS nõuetele. Süstelahuste valmistamisel kasutatavatele lahustitele esitatakse erinõuded.
Steriliseerimine põhjustab ainult mikroorganismide surma; hukkunud mikroobid, nende ainevahetus- ja lagunemissaadused jäävad vette ning neil on pürogeensed omadused, põhjustades tugevaid külmavärinaid ja muid soovimatuid nähtusi. Kõige teravamad pürogeensed reaktsioonid ilmnevad veresoonte, seljaaju ja intrakraniaalsete süstide korral.
Seetõttu tuleks süstelahuseid valmistada vees, mis ei sisalda pürogeenseid aineid.
Kasutusele on võetud meetod pürogeene moodustavate mikroorganismide tuvastamiseks ja sisalduse normide määramiseks enne apteegitööstuse süste- ja infusioonilahuste steriliseerimist, mille kohta on olemas normatiivne ja tehniline dokumentatsioon.
Raviainete oksüdeerumise vältimiseks on vajalik, et kasutatav vesi sisaldaks minimaalses koguses lahustunud hapnikku. Seetõttu on vaja süstimiseks kasutada värskelt keedetud vett.
Süstevesi peab vastama puhastatud vee nõuetele ja olema pürogeenivaba. Seda võib aseptilistes tingimustes säilitada mitte rohkem kui 24 tundi.
Apteekides viiakse süstevee pürogeensuse kontroll ja testimine läbi vähemalt 2 korda kvartalis. Puhastatud vett ja süstevett tuleb kvalitatiivselt analüüsida (proovid võetakse igast silindrist ja igas töökohas torujuhtme kaudu vee tarnimisel) ClІЇ, SO ІЇCaI+ soolade puudumise tuvastamiseks. Steriilsete lahuste valmistamiseks mõeldud vett kontrollitakse lisaks ülaltoodud testidele ka redutseerivate ainete, ammooniumsoolade ja süsinikdioksiidi puudumise suhtes vastavalt kehtiva ülemaailmse fondi nõuetele.
Kord kvartalis saadetakse süstevesi ja puhastatud vesi kontroll- ja analüüsilaborisse täielikuks keemiliseks analüüsiks.
Puhastatud vee ja süstevee kontrolli tulemused tuleks registreerida ajakirjas, mille vorm on toodud Vene Föderatsiooni tervishoiuministeeriumi korralduse nr 214 juhendi 3. lisas.
Nõuded süstevee vastuvõtule, transportimisele ja säilitamisele on toodud korralduse nr 309 juhendi punktis 7.
Süstevee vastuvõtmine peaks toimuma aseptilise üksuse destilleerimisruumis, kus on rangelt keelatud teha töid, mis ei ole seotud vee destilleerimisega, kasutades AE-25, DE-25, AA veedestilleerijaid. -1, A-10, AEVS-4 jne. Nende kaubamärkide veedestillaatorid on varustatud separaatoritega, mis takistavad mikroorganisme sisaldavate veepiiskade sattumist kondensatsioonikambrisse.
Süstevett kasutatakse värskelt valmistatud ja hoitakse temperatuuril 5-10 °C või 80-95 °C suletud anumates, mis on valmistatud materjalidest, mis ei muuda vee omadusi, kaitstes seda mehaaniliste lisandite ja mikrobioloogilise saastumise eest, mitte enam. kui 24 tundi.
Saadud süstevesi kogutakse tööstusliku tootmise steriliseeritud auruga töödeldud kogudesse (erandina klaassilindrid). Kollektsioonidel peab olema selge kiri "Süstevesi", küljes on silt, mis näitab selle kättesaamise kuupäeva, analüüsi numbrit ja inspektori allkirja. Kui kasutatakse korraga mitut kollektsiooni, nummerdatakse need. Süstevee kogumiseks ja säilitamiseks mõeldud mahutid peavad olema märgistatud, mis näitab, et sisu ei ole steriliseeritud.
Lisaks tellimuse nr 309 juhistele on nüüdseks välja töötatud mitu süstevee kvaliteeti reguleerivat FS-i:
FS42-2620-97 "Süstevesi"
FS42-213-96 "Süstevesi ampullides"
FS42-2980-99 "Süstevesi viaalides".
Süstelahuste valmistamisel kasutatakse lahustina ka virsiku-, mandli-, oliivi- ja muid rasvhappeid. Need on madala viskoossusega kergesti liikuvad vedelikud, mis võivad läbida nõela kitsa kanali.
GPC1 nõuab, et süsteõlid oleksid värskest seemnest külmpressitud, hästi veetustatud ja valguvabad. Lisaks on eriti oluline õli happesus. Süstitavate õlide happearv peab olema vähemalt 2,5, vastasel juhul võivad need süstekohas põhjustada valulikkust.
Süstelahuste lahustiks võivad olla ka alkoholid (etüül, bensüül, propüleenglükool, polüetüleenoksiid 400, glütseriin), mõned estrid (bensüülbensoaat, etiooleaat).
Süstelahustina on vastuvõetamatu kasutada vaseliiniõli, mis ei imendu kehasse ja naha alla süstides moodustub mitteimenduvad õlikasvajad.
7) Ravimite ja abiainete valmistamine
Süstelahuste valmistamisel kasutatavad ravimained peavad vastama GF, FS, VFS, GOST, keemiliselt puhta kvalifikatsiooni nõuetele. (keemiliselt puhas) ja analüütiline. (analüüsi jaoks puhas). Mõningaid aineid puhastatakse täiendavalt ja neid toodetakse kõrgendatud puhtusastmega kvalifikatsiooniga "Süstimiseks hea". Viimases sisalduvad lisandid võivad avaldada patsiendi organismile toksilist mõju või vähendada süstelahuse stabiilsust.
Glükoos ja želatiin (soodne keskkond mikroorganismide arenguks) võivad sisaldada pürogeenseid aineid.Seetõttu määratakse neile katseannustes pürogeenid vastavalt artiklile GFKh1 "Pürogeensuskatse". Glükoos ei tohiks anda pürogeenset toimet 5% lahuse lisamisel kiirusega 10 mg / kg küüliku massi kohta, želatiin 10% lahuse lisamisega.
Bensüülpenitsilliini kaaliumsoola testitakse ka pürogeensuse ja toksilisuse suhtes.
Mõnede ravimite puhul tehakse puhtuse osas täiendavaid uuringuid: kaltsiumkloriidi kontrollitakse etanoolis ja rauasisalduses lahustumise suhtes, heksametüleentetramiin - amiinide, ammooniumisoolade ja kloroformi puudumise suhtes; kofeiin-naatriumbensoaat - orgaaniliste lisandite puudumisel (lahus ei tohiks kuumutamisel muutuda häguseks ega sadestuda 30 minuti jooksul); magneesiumsulfaat süstimiseks ei tohiks sisaldada mangaani ja muid aineid, mis on märgitud regulatiivses dokumentatsioonis.
Mõned ained mõjutavad süstelahuste stabiilsust. Näiteks keemiliselt puhas naatriumvesinikkarbonaat. ja analüütiline kvaliteet, vastab GOST 4201-66 nõuetele, samuti "Süstimiseks hea", peab vastu pidama täiendavatele 5% lahuse läbipaistvuse ja värvituse nõuetele, kaltsiumi ja magneesiumi ioonide sisaldus ei tohiks olla suurem kui 0,05%, vastasel korral lahuse termilisel steriliseerimisel vabaneb nende katioonide karbonaatide opalestsents. Eufilin süstelahuses peaks sisaldama suurendatud kogust etüleendiamiini (18-22%), mida kasutatakse selle aine stabilisaatorina koguses 14-18% lahustes. suukaudne manustamine ja taluvad täiendavaid lahustumiskatseid. Naatriumkloriid (keemiliselt puhas), mis on toodetud vastavalt standardile GOST 4233-77, peab vastama ülemaailmse fondi nõuetele, kaaliumkloriid (keemiliselt puhas) peab vastama GOST 4234-65 ja ülemaailmse fondi nõuetele. Analüütilise puhtusega naatriumatsetaat. peab vastama GOST 199-68 nõuetele, naatriumbensoaat ei tohi sisaldada rohkem kui 0,0075% rauda. Tiamiinbromiidi süstelahus peab läbima täiendavad läbipaistvuse ja värvituse testid.
Süstelahuste valmistamiseks kasutatavaid ravimaineid hoitakse eraldi kapis steriilsetes kangides, mis on suletud jahvatatud korgi ja kirjaga "Steriilsetele ravimvormidele". Kuumakindlad ained steriliseeritakse enne varda täitmist termiliselt.
Varred pestakse ja steriliseeritakse enne täitmist. Igale kangile tuleb kinnitada silt, millel on märgitud: seerianumber, tootja ettevõte, kontroll- ja analüüsilabori analüüsi number, kõlblikkusaeg, täitmise kuupäev ja kangi täitja allkiri. Täitmine ja aegumiskuupäevade kontroll toimub vastavalt Vene Föderatsiooni Tervishoiuministeeriumi 16. juuli 1997. a korraldusele nr 214.
Süstelahused valmistatakse massi-mahukontsentratsioonis. Lahuste valmistamiseks kaalutakse vajalik kogus ravimainet ja lahustatakse see mõõtenõus süstevees, misjärel see reguleeritakse vajaliku mahuni.
Mõõteanuma puudumisel määratakse lahuse valmistamiseks vajalik kogus arvutuste teel, kasutades antud kontsentratsiooni tiheduse väärtust või mahulaiendustegurit (VFR), mille all mõistetakse ruumala suurenemist, kui 1 g aine on lahustunud.
CMR-tabel on toodud Vene Föderatsiooni tervishoiuministeeriumi korraldusega nr 308 kinnitatud apteekides vedelate ravimvormide valmistamise juhendi 9. lisas.
Kristalliseeritud vett sisaldavate preparaatide puhul arvutage ümber aine kogus veevaba preparaadi kohta.
Rangelt keelatud on samal töölaual üheaegselt valmistada mitut erineva nimetuse või ühe nimetusega, kuid erineva kontsentratsiooniga steriilset lahust, mis sisaldavad ravimaineid.
Lahuseid, milles osmootne rõhk on võrdne vere osmootse rõhuga, nimetatakse isotoonilisteks. Vereplasmas, lümfis, pisara- ja seljaajuvedelikus on konstantne osmootne rõhk, mida säilitavad spetsiaalsed osmoretseptorid. Erineva osmootse rõhuga süstelahuste suurte koguste sattumine vereringesse võib viia osmootse rõhu nihkeni ja põhjustada tõsiseid tagajärgi. Seda seletatakse järgmiste asjaoludega. Rakumembraanidel, nagu teate, on poolläbilaskvus, st nad läbivad vett, ei lase läbi paljusid selles lahustunud aineid. Kui väljaspool rakku on vedelik, mille osmootne rõhk on erinev kui raku sees, siis liigub vedelik rakku (eksoosmoos) või rakust välja (endoosmoos), kuni kontsentratsioon ühtlustub. Kui verre viiakse kõrge osmootse rõhuga lahus (hüpertooniline lahus), siis selle tulemusena suunatakse neid ümbritsevas plasmas erütrotsüütide vedelik plasmasse, samas kui erütrotsüüdid, kaotades osa veest, kahaneb (plasmolüüs). Vastupidi, kui süstida madala osmootse rõhuga lahust (hüpotooniline lahus), läheb vedelik raku sisse, erütrotsüüdid paisuvad, kest võib lõhkeda ja rakk sureb (toimub hemolüüs). Nende osmootsete nihete vältimiseks tuleks vereringesse viia lahused, mille osmootne rõhk on võrdne vere, tserebrospinaal- ja pisaravedeliku osmootse rõhuga, s.o. 7,4 atm ja vastab 0,9% naatriumkloriidi lahuse osmootsele rõhule.
Ravimite isotoonilisi kontsentratsioone lahustes saab arvutada mitmel viisil:
- 1. Van't Hoffi seaduse järgi arvutamine
- 2. Krüoskoopiline meetod.
- 3. Mõnikord kasutatakse isotoonilise kontsentratsiooni arvutamiseks graafilist meetodit, mis võimaldab väljatöötatud diagrammide (nonogrammide) abil kiiresti, kuid mõningase lähendusega määrata ravimilahuse isotooniliseks muutmiseks vajaliku aine koguse.
Nende meetodite puuduseks võib pidada seda, et isotoonilise kontsentratsiooni arvutused tehakse ühe komponendi kohta või on teise aine massi arvutamine liiga tülikas. Ja sellepärast ühekomponentsete lahenduste valik ei ole nii suur ning üha enam kasutatakse kahe- või enamakomponentseid ettekirjutusi, isotoonilise ekvivalendi abil on arvutusi palju lihtsam teha. Hetkel muid arvutusmeetodeid ei kasutata.
Naatriumkloriidi isotooniline ekvivalent on naatriumkloriidi kogus, mis tekitab samadel tingimustel osmootse rõhu, mis on võrdne 1 g aine osmootse rõhuga. Teades naatriumkloriidi ekvivalenti, saab isotoniseerida mis tahes lahuseid, samuti saab määrata nende isotoonilisi kontsentratsioone.
Naatriumkloriidi isotooniliste ekvivalentide tabel on toodud SPXI väljaande 2. numbris.
Arvutuse näide: Rp.:
Natrii chloridiq.s. ut f. sol. Isotoonilised 1000 ml
Isotoonilise lahuse valmistamiseks ainult naatriumkloriidist peate 1 liitri lahuse valmistamiseks võtma seda 9 g (naatriumkloriidi isotooniline kontsentratsioon on 0,9%). GFXI tabeli järgi määrame, et dikaiini naatriumkloriidi isotooniline ekvivalent on 0,18 g.
See tähendab et
- 1 g dikaiini võrdub 0,18 g naatriumkloriidiga ja
- 3 g dikaiini - 0,54 g naatriumkloriidi.
Seetõttu on naatriumkloriidi retsepti kohaselt vaja võtta: 9,0 - 0,54 \u003d 8,46 g.
Süstelahuste valmistamisel (eriti kuumsteriliseerimisel) ja hilisemal ladustamisel on võimalik lahustuvate ravimite osaline lagunemine. Samal ajal toimuvad keerulised ja sageli ebapiisavalt uuritud protsessid. Lagunemiskiirus ei sõltu ainult temperatuurist, vaid ka keskkonna pH-st ja pakendi omadustest.
Resistentsuse suurendamiseks üksikute süstelahuste suhtes lisatakse sobivaid stabilisaatoreid, säilitusaineid, antioksüdante, emulgaatoreid ja muid eraartiklites nimetatud abiaineid.
Abiainetena askorbiin, vesinikkloriid, viin, sidrun, äädikhape, naatriumkarbonaat, naatriumvesinikkarbonaat, naatriumhüdroksiid, naatrium- või kaaliumsulfit, vesiniksulfit või metasulfit, naatriumteosulfaat, naatriumtsitraat, naatriumfosfaat mono- ja diasendatud, naatriumkloriid, hüdroksübensoehappe metüülester, rongaliit, etüleendiamiinhappe polüvinodiamiintetrasool, klorobutanool, kresool, fenool.
Lisatud kogus abiaine, välja arvatud juhul, kui eraartiklites on märgitud, ei tohiks ületada järgmisi kontsentratsioone: sarnase klorobutanooli, kresooli, fenooli puhul - kuni 0,5%; vääveldioksiid või samaväärne kogus kaalium- või naatriumsulfiti, bisulfiti või metasulfiti - kuni 0,2%.
Raviained intrakavitaarseks, intrakardiaalseks, silmasiseseks või muudeks süstideks, millel on juurdepääs tserebrospinaalvedelik, samuti ühekordse annusena, mis ületab 15 ml, ei tohiks sisaldada säilitusaineid.
Stabilisaatori valik sõltub peamiselt süstelahustes sisalduvate ravimite omadustest.
Stabiliseerimise küsimuses jagatakse ravimained laias laastus kolme rühma:
- 1. Nõrkade aluste ja tugevate hapete soolade lahused, mis stabiliseeritakse hapete - vesinikkloriid-, viin-, sidrun-, äädikhappe - lahuse lisamisega.
- 2. Tugevate aluste ja nõrkade hapete soolade lahused, mis on stabiliseeritud naatriumhüdroksiidi, naatriumkarbonaadi lahuse lisamisega.
- 3. Kergesti oksüdeeruvate ravimite lahused, mis on stabiliseeritud antioksüdantide lisamisega.
a) Nõrkade aluste ja tugevate hapete soolade lahuste stabiliseerimine
Sellesse rühma kuuluvad alkaloidide soolade ja sünteetiliste lämmastikaluste lahused, millel on süstelahuste hulgas oluline koht.
Nende soolade lahused on neutraalsed või kergelt happelised. Lahustumisel toimub soola hüdrolüüs ja pH kerge tõus põhjustab sademete teket, mis võib olla põhjustatud klaasileeliste olemasolust.
Nende muutuste vältimiseks vastavalt GPXI-le on enamik neist lahendustest stabiliseeritud 0,1 N-ga. vesinikkloriidhappe lahus. Mille ülesandeks on neutraliseerida klaasist eralduvat leelist ja langetada lahuse pH-d happepoolele.
Kogus vesinikkloriidhappest lahuse stabiliseerimiseks vajalik kogus sõltub ravimainete omadustest. Kõige sagedamini lisage 10 ml 0,1 N. HCl lahus 1 liitri stabiliseeritud lahuse kohta, mis vastab 0,001 N. vesinikkloriidhappe lahus (pH 3-4). Sellist HCl kogust soovitatakse kasutada dikaiini, dibasooli, kokaiinvesinikkloriidi, strühniinsulfaadi ja muude süstelahuste jaoks.
Ravimi stabiilsuse optimaalse pH saavutamiseks võib lisada väiksemaid või suuremaid koguseid 0,1 N. HCl. GFXI järgi stabiilse 0,5-1-2% novokaiini süstelahuse saamiseks on vaja lisada 0,1 n. HCl lahus pH väärtuseni 3,8-4,5, mis vastab 3,4 ja 9 ml 0,1 n. vesinikkloriidhape 1 liitri lahuse kohta. Novokaiini (1-2%) stabiilse lahuse valmistamiseks isotoonilises naatriumkloriidi lahuses lisage 1 liitri kohta 5 ml 0,1 HCl lahust.
Näidatud koguste HCl lisamisel saadakse minimaalse koguse vesinikkloriidiga lahused. Sellise lahuse kasutuselevõtt ei mõjuta keha.
Praktilise tähtsusega on 0,1 N lahuse valmistamine ja ladustamine. HCl. Apteekides on doseerimise ja säilitamise hõlbustamiseks soovitav valmistada 0,01 n. HCl lahus vastavalt retseptile: 0,42 ml vesinikkloriidhapet lahjendatuna 100 ml vees. Valmistatud lahus valatakse 10 ml neutraalse klaasi pudelitesse ja steriliseeritakse küllastunud auruga rõhu all temperatuuril 120 °C 8 minutit. Lahust kasutatakse mitmekordselt. Stabilisaatori kõlblikkusaeg ei ületa 5 päeva.
AT vesilahused nõrkade hapete ja tugevate aluste soolad hüdrolüüsuvad kergesti, moodustades keskkonnas kergelt leeliselise reaktsiooni, mis põhjustab vähelahustuvate sademete moodustumist.
Selliste lahuste stabiliseerimiseks kasutatakse 0,1 N. naatriumhüdroksiidi lahus ja mõnikord naatriumkarbonaat koguses 2–4 g ainet 1 liitri lahuse kohta.
Selle meetodiga stabiliseeritud ainete hulka kuuluvad sellised ained nagu naatriumteosulfaat, kofeiin-naatriumbensoaat, teofeliin jne.
Kergesti oksüdeerivate ainete hulka kuuluvad askorbiinhape, adrenaliinvesiniktartraat, etüleenmorfiinvesinikkloriid, vikasool, novokaiin, fenoftivasiini derivaadid ja muud raviained.
Nende ainete süstelahuste valmistamisel toimub oksüdatsioon vees sisalduva hapniku juuresolekul ja lahuse kohal. Selle tulemusena moodustuvad lahustes oksüdatsiooniproduktid, mis on sageli mürgisemad või füsioloogiliselt mitteaktiivsed. Oksüdatsioon suureneb oluliselt valguse, soojuse, pH väärtuse, hapniku mõjul.
Kergesti oksüdeeruvate ainete stabiliseerimiseks kasutatakse erineva toimemehhanismiga antioksüdante. Nende hulka kuuluvad madala valentsusega väävlit sisaldavad ained (rongaliit, unitool, naatriummetabisulfit jne), raskemetalle siduvad kompleksoonid (ETDA, Trilon B, kaltsiumteetatsiin), kõrgmolekulaarsed ained (polüglütsiin, propüleenglükool jne). Praegu arendatakse võimalust kasutada kompleksseid stabilisaatoreid ning katsetatakse uute antioksüdantide ohutust.
Glükoosilahuste stabiliseerimine väärib erilist tähelepanu. Varem valmistati glükoosilahused Weibeli stabilisaatoriga, mis koosnes 5,2 g naatriumkloriidist, 4,4 lahjendatud 8,3% vesinikkloriidhappest ja veest 1 liitri lahuse kohta. Kuid praegu on vastavalt Vene Föderatsiooni tervishoiuministeeriumi poolt 19. juunil 1997 heaks kiidetud MU "Glükoosilahuste tehnoloogia, kvaliteedikontroll ja säilivusaeg 5%, 10%, 20% apteekides tehtud süstide jaoks". lisaks tellimusele nr 214 valmistatakse etteantud kontsentratsioonist kõrgemaid glükoosilahuseid ilma stabilisaatorita.
Pärast süstelahuse valmistamist ja enne selle steriliseerimist allutatakse sellele tingimata täielik keemiline kontroll, sealhulgas selle komponentide kvalitatiivne ja kvantitatiivne analüüs, pH määramine, isotoonilised ja stabiliseerivad ained.
Lisaks on võimalik täiendav küsitluskontroll pärast lahuse valmistamist.
Kontrolli tulemused registreeritakse logivormil, mis on toodud Vene Föderatsiooni tervishoiuministeeriumi 16. juuli 1997. aasta korraldusega nr 214 kinnitatud kvaliteedikontrolli juhendi lisas 2.
See süstelahuste valmistamise etapp viiakse läbi ainult täieliku keemilise analüüsi rahuldavate tulemustega.
1) Filtreerimine ja villimine, korkimine
Filtreerimine viiakse läbi, et vabastada süstelahused mehaanilistest lisanditest.
Filtrisüsteemi usaldusväärseks valikuks on soovitav analüüsida järgmist teavet puhastustehnoloogia kohta:
- - filtreeritud keskkonna olemus (nimetus, koostisained, tihedus, viskoossus, kontsentratsioon);
- - reostuse olemus (osakeste suurus);
- - nõuded filtraadile (visuaalne läbipaistvus või muu);
- - kasutatud seadmed ja filtrielemendid, näidates ära tüübi, kaubamärgi, materjali, peamised toimivusnäitajad vastavalt passile.
Filtraadi esimesed osad filtreeritakse uuesti.
Lahuse filtreerimine kombineeritakse selle samaaegse täitmisega ettevalmistatud klaaspudelitesse. Filtreerimise ja täitmise ajal ei tohi töötajad tühjade või täis viaalide kohale kummarduda. Optimaalne laminaarse õhuvoolu täitmine ja sulgemine, kasutades sobivat varustust.
Süstelahuste filtreerimiseks kasutatakse klaasfiltriga (poori suurus 3-10 μm) filtrilehtreid. Sel juhul kasutatakse kahe kujundusega installatsioone:
- 1. statiivi tüüpi aparaat
- 2. Karusselli tüüpi aparaat.
Lisaks kasutatakse vedelike filtreerimis- ja villimisseadmeid UFZh-1 ja UFZh-2, mille abil saab korraga filtreerida mitut lahust.
Keskendudes suurte süstelahuste koguste filtreerimisele, kasutatakse filtreid, mis töötavad vaakumis "seene" põhimõttel, kasutades ümberpööratud Büncheri lehtrit. Lehtri põhja on üksteise peale laotud filtrimaterjal, mis tagab põhjalikuma filtreerimise.
Filtreerimismaterjalina kasutatakse kombineeritud filtreid kombineerituna erinevate filtreerimismaterjalidega (filterpaber, marli, vatt, puuvillane kalikorühm, vöö, looduslik siidkangas).
Tähelepanu tuleb pöörata asjaolule, et praegu kasutatakse üha enam mikrofiltrimise meetodit läbi membraanfiltrite.
Mikrofiltreerimine on protsess, mille käigus eraldatakse kolloidlahused ja mikrosuspensioonid rõhu all. Sel juhul eraldatakse osakesed suurusega 0,2-10 mikronit (anorgaanilised osakesed, suured molekulid). Tavaline filtrimaterjal laseb need osakesed läbi, mis on väga ohtlik, kuna. nad on kapillaare mitteläbilaskvad ja kalduvad konglomeratsioonile.
Mikrofiltratsiooni kasutamine võimaldab visuaalse kontrolliga vabaneda mehaanilistest lisanditest ja vähendada mikroobide koguarvu. See on tingitud asjaolust, et membraanid ei säilita mitte ainult osakesi, mis on suuremad kui poorid, vaid ka väiksema suurusega osakesed. Selles protsessis mängivad olulist rolli järgmised mõjud: 1) kapillaarefekt; 2) adsorptsiooni nähtus; 3) elektrostaatilised jõud; 4) Van der Waalsi väed.
Kõige sagedamini kasutatavad filtrid on välismaised kaubamärgid - MELIPORD, SARTERIDE, SINPOR jt. Samuti kasutatakse sageli kodumaise kaubamärgi VLADIPOR filtreid, mis on erineva paksusega peeneks poorsed valget värvi tselluloosatsetaatkiled.
Lahuste filtreerimine membraani mikrofiltrite abil hõlmab membraaniüksuse kasutamist, mis on keeruline seade, mis koosneb membraanihoidjatest ja muudest abiseadmetest.
Pärast lahuste täitmist samaaegse filtreerimisega suletakse viaalid kummikorkidega (kaubamärgid, vt “Tasside ja sulgurite valmistamine”) ning läbivad esmase visuaalse kontrolli mehaaniliste lisandite puudumise suhtes vastavalt kvaliteedikontrolli juhendi 8. lisale. apteekides toodetud ravimite kohta, kinnitatud Vene Föderatsiooni tervishoiuministeeriumi 16. juuli 1997. a korraldusega nr 214.
2) Esmane kontroll mehaaniliste lisandite puudumisel.
Mehaaniliste inklusioonide all mõistetakse pidevalt liikuvaid lahustumatuid aineid, välja arvatud gaasimullid, mis kogemata lahustes esinevad. Esmane kontroll viiakse läbi pärast lahuse filtreerimist ja pakkimist. Iga pudel või viaal lahusega vaadatakse üle. Mehaaniliste lisandite tuvastamisel lahus filtreeritakse ja kontrollitakse uuesti, korgitakse, märgistatakse ja steriliseeritakse Membraaniga mikrofiltreerimisega lahuste puhul on lubatud selektiivne esmane kontroll mehaaniliste lisandite puudumise suhtes.
Kontrolli viib läbi proviisor-tehnoloog järgides kõiki läbiviimise tingimusi ja meetodeid.
Lahenduste vaatamiseks peaks olema spetsiaalselt varustatud töökoht, mis on kaitstud otsese päikesevalguse eest. Juhtimine toimub "Seade lahuse mehaaniliste lisandite puudumise jälgimiseks" (UK-2), lubatud on kasutada must-valget ekraani, mis on valgustatud nii, et valguse sisse ei pääseks. inspektori silmad otse selle allikast.
Lahenduse juhtimine toimub palja silmaga vaatamisega mustvalgetel taustadel, mida valgustab 60 W elektriline mattlamp või 20 W luminofoorlamp; värviliste lahenduste puhul vastavalt 100 W ja 30 W. Kaugus silmadest vaadeldava objektini peaks olema 25-30 cm ja optilise vaatetelje nurk valguse suuna suhtes peaks olema umbes 90º. Vaatejoon peaks olema suunatud allapoole, pea püsti.
Proviisor-tehnoloogil peab nägemisteravus olema võrdne ühega. Vajadusel korrigeeritud prillidega.
Katsetatud pudelite või viaalide pind peab olema väljastpoolt puhas ja kuiv. Olenevalt pudeli või viaali mahust vaadatakse korraga ühest pudelist kuni 5 tk. Pudelid või viaalid võetakse ühe või mõlema käega kaelast, viiakse kontrolltsooni, pööratakse sujuvate liigutustega tagurpidi ja vaadatakse mustvalgel taustal. Seejärel pööravad nad sujuvate liigutustega ilma raputamiseta selle algsesse asendisse "tagurpidi" ja vaatavad seda ka mustvalgel taustal.
Kontrollaeg on vastavalt:
üks pudel mahuga 100-500 ml - 20 sek;
kaks pudelit mahuga 50-100 ml - 10 sekundit;
kahest kuni viie pudeli mahuga 5-50 ml - 8-10 sek.
Määratud kontrollaeg ei sisalda abitoimingute aega.
3) Korgistamine ja märgistamine.
Kummist korgiga suletud süstelahustega viaalid rullitakse pärast rahuldavat kontrolli mehaaniliste lisandite puudumise suhtes metallkorgiga.
Selleks kasutatakse 12-14 mm läbimõõduga sälku (ava) K-7 tüüpi alumiiniumkorke.
Pärast viaalides jooksmist kontrollitakse sulguri kvaliteeti: kontrollimisel ei tohi metallkorki käega kerida ja viaali ümberpööramisel ei tohi lahus välja voolata. Seejärel märgistatakse pudelid ja viaalid allkirjaga, tembeldades korgile või kasutades metallist märke, mis näitavad lahuse nimetust ja selle kontsentratsiooni.
Steriliseerimine on elusate mikroorganismide ja nende eoste täielik hävitamine objektis. Steriliseerimisel on suur tähtsus kõigi ravimvormide ja eriti süstepreparaatide valmistamisel. Sel juhul tuleb klaasnõud, abimaterjal, lahusti ja valmislahus steriliseerida. Seega peaks süstelahuste valmistamise töö algama steriliseerimisega ja lõppema steriliseerimisega.
SPXI määratleb steriliseerimise kui protsessi, mille käigus hävitatakse või eemaldatakse objektilt kõikvõimalikud mikroorganismid kõigis arenguetappides.
Steriliseerimisprotsessi keerukus seisneb ühelt poolt suures elujõulisuses ja paljudes mikroorganismide hulgas, teiselt poolt paljude ravimainete ja ravimvormide termilises labiilsuses või võimetuses kasutada muid steriliseerimismeetodeid. põhjuste arv. Siit tulenevad nõuded steriliseerimismeetoditele: säilitada ravimvormide omadused ja vabastada need mikroorganismidest.
Apteekides, eriti tervishoiuapteekides peaksid olema mugavad kasutada steriliseerimismeetodid, mille koostises moodustavad süstelahused kuni 60-80%.
Annustamisvormide tehnoloogias kasutatakse erinevaid steriliseerimise meetodeid: termilised meetodid, steriliseerimine filtreerimise teel, kiirgussteriliseerimine, keemiline steriliseerimine.
Termilise steriliseerimise meetodid hõlmavad survestatud auruga steriliseerimist ja õhuga steriliseerimist, voolava auruga steriliseerimine on GFXI-st välja jäetud.
See steriliseerimismeetod viiakse läbi kuuma õhuga õhusterilisaatoris temperatuuril 180-200ºC. Sel juhul surevad kõik mikroorganismide vormid valguliste ainete pürogeneetilise lagunemise tõttu.
Õhusteriliseerimise efektiivsus sõltub temperatuurist ja ajast. Objektide ühtlane kuumutamine sõltub soojusjuhtivuse astmest ja õigest asukohast steriliseerimiskambri sees, et tagada kuuma õhu vaba ringlus. Steriliseeritavad esemed tuleb pakendada vastavatesse anumatesse või suletuna ja asetada vabalt sterilisaatorisse. Kuna õhul ei ole kõrget soojusjuhtivust, toimub steriliseeritud esemete soojenemine üsna aeglaselt, mistõttu tuleks laadimine teha soojendamata sterilisaatorites või siis, kui temperatuur nende sees ei ületa 60ºC. Steriliseerimiseks soovitatud aega tuleks arvestada sterilisaatoris kuumutamise hetkest temperatuurini 180-200°C.
Õhusteriliseerimise meetodit kasutatakse kuumakindlate ravimite, õlide, rasvade, lanoliini, vaseliini, vaha, aga ka klaasi, metalli, silikoonkummi, portselani, filtritega steriliseerimisseadmete, väikeste klaas- ja metallesemete steriliseerimiseks.
Seda meetodit ei kasutata lahuste steriliseerimiseks.
1) Auruga steriliseerimine.
Selle steriliseerimismeetodiga kaasneb kombineeritud toime mikroorganismidele. kõrge temperatuur ja niiskus. Usaldusväärne steriliseerimismeetod on steriliseerimine küllastunud auruga ülerõhul, nimelt: rõhk 0,11 MPa (1,1 kgf / cm²) ja temperatuur 120 ° C või rõhk 0,2 MPa (2,2 kgf / cm²) ja temperatuur 132 ° C. ° C.
Küllastunud aur on aur, mis on tasakaalus vedelikuga, millest see moodustub. Küllastunud auru märk on selle temperatuuri range sõltuvus rõhust.
Rõhu all auruga steriliseerimine toimub aurusterilaatorites.
Termostabiilsete ravimilahuste puhul on soovitatav steriliseerida auruga 120°C. Steriliseerimise kokkupuuteaeg sõltub ainete füüsikalis-keemilistest omadustest ja lahuse mahust.
Süstitavate ravimainete steriliseerimine toimub hermeetiliselt suletud, eelnevalt steriliseeritud viaalides.
See meetod steriliseerib ka rasvu ja õlisid hermeetiliselt suletud anumates temperatuuril 120 ° C 2 tundi; klaasist, portselanist, metallist, sidemetest ja abimaterjalidest (vatt, marli, sidemed, hommikumantlid, filterpaber, kummikorgid, pärgament) valmistatud tooted - kokkupuuteaeg 45 minutit temperatuuril 120 ° C või 20 minutit temperatuuril 132°C.
AT erandjuhtudel steriliseeritud temperatuuril alla 120°C. Steriliseerimisrežiim peab olema põhjendatud ja täpsustatud GFXI eraartiklites või muus regulatiivses ja tehnilises dokumentatsioonis.
Termilise steriliseerimise meetodite tõhususe kontrollimine toimub termomeetritega instrumentide, samuti keemiliste ja bioloogiliste meetodite abil.
Keemiliste testidena kasutatakse mõningaid aineid, mis teatud steriliseerimisparameetrite juures muudavad oma värvi või füsioloogilist olekut. Näiteks bensoehape (sulamistemperatuur 122-124,5 ° C), sahharoos (180 ° C) ja muud ained.
Bakterioloogiline tõrje toimub objekti steriliseerimise teel, seemendatakse katsemikroobidega, kasutada võib aiamullaproove.
Seda steriliseerimismeetodit kasutatakse apteekides kõige sagedamini süstelahuste steriliseerimiseks, kusjuures tuleb arvestada järgmiste nõuetega:
- 1. Steriliseerimine tuleb läbi viia hiljemalt 3 tunni jooksul alates lahuse valmistamise hetkest;
- 2. Steriliseerimine toimub ainult üks kord, korduv steriliseerimine ei ole lubatud;
- 3. Täidetud kastidele või pakenditele peab olema märgitud sisu nimetus ja steriliseerimise kuupäev;
- 4. Termilise steriliseerimise kontrolli läbiviimine süstelahuste steriliseerimise ajal on kohustuslik;
- 5. Steriliseerimist on õigus teha ainult eriväljaõppe ja teadmiste kontrolli läbinud isik, kellel on seda tõendav dokument.
- 2) Steriliseerimine filtreerimise teel.
Mikroobirakke ja eoseid võib pidada väga väikese (1–2 µm) läbimõõduga lahustumatuteks moodustisteks. Sarnaselt teistele kandmistele saab neid vedelikust eraldada mehaaniliselt – filtreerides läbi peenpoorsete filtrite. See steriliseerimismeetod sisaldub ka termolabiilsete ainete lahuste steriliseerimiseks mõeldud SPXI-s.
3) Kiirgussteriliseerimine.
Kiirgusenergial on kahjulik mõju elusorganismide, sealhulgas erinevate mikroorganismide rakkudele. Kiirguse steriliseeriva toime põhimõte põhineb võimel tekitada elusrakkudes teatud neeldunud energiadooside juures muutusi, mis paratamatult põhjustavad nende surma metaboolsete häirete tõttu. Mikroorganismide tundlikkus ioniseeriva kiirguse suhtes sõltub paljudest teguritest: niiskuse olemasolust, temperatuurist jne.
Kiirgussteriliseerimine on tõhus suurtes tööstustes.
4) Keemiline steriliseerimine.
See meetod põhineb mikroorganismide kõrgel eritundlikkusel erinevate kemikaalide suhtes, mille määrab nende kesta ja protoplasma füüsikalis-keemiline struktuur. Ainete antimikroobse toime mehhanismi pole siiani hästi mõistetud. Arvatakse, et mõned ained põhjustavad raku protoplasma koagulatsiooni, teised toimivad oksüdeerivate ainetena, mitmed ained mõjutavad raku osmootseid omadusi, paljud keemilised tegurid põhjustavad mikroobiraku surma oksüdatiivsete ja muud ensüümid.
Keemilist steriliseerimist kasutatakse riistade, abitarvikute, klaasnõude, portselani, metalli steriliseerimiseks, samuti kasutatakse seinte ja seadmete desinfitseerimiseks.
Süstimise steriilsuse kontroll ravimid toodetud apteekides, Vene Föderatsiooni Tervishoiuministeeriumi 21. oktoobri 1997. a korraldusega nr 309. teostavad tervishoiuasutused. Viimane on kohustatud kontrollima süstelahuseid vähemalt kaks korda kvartalis, silmatilgad ja süstevesi steriilsuse tagamiseks; teostama kord kvartalis SPXI nõuete kohaselt apteekides pürogeensete ainete süstevee ja süstelahuste selektiivset kontrolli.
Süstelahuste kvaliteedikontroll peaks hõlmama kõiki nende valmistamise etappe alates ravimainete apteeki jõudmisest kuni ravimvormina vabanemiseni.
Vastavalt 16. juuli 1997. a korraldusega nr 214 kinnitatud Apteegis toodetavate ravimite kvaliteedikontrolli juhendile viiakse ebakvaliteetsete ravimite apteeki sattumise vältimiseks läbi vastuvõtukontroll. , mis seisneb käesolevate ravimite vastavuse kontrollis järgmistele näitajatele: " Kirjeldus", "Pakend", "Märgistus"; erinevate dokumentide vormistamise õigsuse ning vastava tootja sertifikaatide ja muu ravimi kvaliteeti kinnitava dokumentatsiooni olemasolu kontrollimisel. Samas peab süste- ja infusioonilahuste valmistamiseks mõeldud ravimainetega pakendi etiketil olema märge “Sobib süstimiseks”.
Tootmisprotsessi ajal peab olema kirjalik, organoleptiline kontroll ja kontroll vabastamise ajal - kohustuslik; küsimustik, füüsikaline - valikuliselt ja täielik keemiline vastavalt korralduse nr 214 punkti 8 nõuetele.
Kirjaliku kontrolli all, v.a üldreeglid passide registreerimisel tuleb meeles pidada, et süste- ja infusioonilahustele lisatavate isotoniseerivate ja stabiliseerivate ainete kontsentratsioon ja maht (mass) tuleb märkida mitte ainult passidesse, vaid ka retseptidesse.
Küsitluskontroll viiakse läbi valikuliselt pärast mitte rohkem kui viie ravimvormi valmistamist.
Organoleptiline kontroll seisneb ravimvormi kontrollimises vastavalt näidustustele:
- - kirjeldus (välimus, värvus, lõhn);
- - homogeensus;
- - nähtavate mehaaniliste lisandite puudumine (vedelates ravimvormides).
Füüsiline kontroll seisneb ravimvormi massi või mahu, selles ravimvormis sisalduvate üksikute komponentide koguse ja massi kontrollimises.
Samal ajal kontrollitakse iga steriliseerimist vajava ravimilahuse partii pärast pakendamist ja enne steriliseerimist. Kontrollimise käigus kontrollitakse ka pakendi kvaliteeti (alumiiniumkorki ei tohi käsitsi kerida ja viaali ümberpööramisel ei tohi lahus välja voolata).
Enne steriliseerimist alluvad kõik süste- ja infusioonilahused täielikule keemilisele kontrollile, sealhulgas pH väärtuse, isotoniseerivate ja stabiliseerivate ainete määramisele.
Kõik süste- ja infusioonilahuste valmistamise etapid peaksid kajastuma süste- ja infusioonilahuste valmistamise üksikute etappide kontrolli tulemuste registris.
1) Sekundaarne kontroll mehaaniliste lisandite puudumisel
Pärast steriliseerimist kontrollitakse suletud lahuseid mehaaniliste lisandite puudumise suhtes teisese kontrolliga. Tingimuste ja kontrollitehnika kohta vt "Esmane kontroll mehaaniliste lisandite puudumisel". Samal ajal kontrollitakse samaaegselt ka viaali täitmise täielikkust ja sulguri kvaliteeti.
2) Täielik keemiline kontroll
Täieliku keemilise kontrolli läbiviimiseks pärast steriliseerimist võetakse igast ravimipartiist üks viaal. Sarjaks loetakse ühes konteineris saadud tooteid.
Täielik keemiline kontroll hõlmab lisaks kvaliteedi- ja kvantifitseerimine toimeaineid, samuti pH väärtuse määramine. Stabiliseerivaid ja isotoniseerivaid aineid kontrollitakse kehtivas regulatiivses dokumentatsioonis (Juhised) ette nähtud juhtudel.
3) Abielu
Steriilsed lahendused loetakse tagasilükatuks, kui need ei vasta regulatiivse dokumentatsiooni nõuetele välimus, pH väärtus; sissetulevate ainete autentsus ja kvantitatiivne sisaldus; nähtavate mehaaniliste lisandite olemasolu; lubamatud kõrvalekalded lahuse nimimahust; kinnitussulguri rikkumised; väljastamiseks mõeldud ravimite registreerimise kehtivate nõuete rikkumised.
Süstimiseks mõeldud ravimained, nagu ka muud ravimvormid, väljastatakse etiketiga. Sel juhul peab siltidel olema valgel taustal sinine signaalriba ja selged kirjad: "Süstimiseks", "Steriilne", "Hoida lastele kättesaamatus kohas", trükitud tüpograafiliselt. Sildid ei tohi ületada 120 x 50 mm. Lisaks peavad siltidel olema järgmised andmed:
- - embleem
- - tootja asutuse asukoht
- - tootjaasutuse nimi
- - Haigla nr.
- - osakonna nimi
- - manustamisviis (intravenoosne, intravenoosne, tilguti, intramuskulaarne)
- - valmistamise kuupäev
- - säilitusaeg
- - Analüüs nr.
- - keedetud
- - kontrollitud
- - jäi vahele
Süstelahuste säilitamine
Süstimiseks mõeldud ravimvorme tuleb hoida jahedas, pimedas kohas, eraldi kapis või isoleeritud ruumis ning arvestades konteineri omadusi (haprus), kui pakendil ei ole märgitud teisiti. Plasma asendavaid ja detoksifitseerivaid lahuseid hoitakse isoleeritult temperatuuril 0–40 °C valguse eest kaitstud kohas. Mõnel juhul on lahuse külmutamine lubatud, kui see ei mõjuta ravimi kvaliteeti (Vene Föderatsiooni tervishoiuministeeriumi korraldus nr 377).
Süstitavad ravimvormid on ravimvormide rühm, mis viiakse kehasse naha ja limaskestade terviklikkuse rikkumisega õõnsa nõela ja süstla abil või nõelavabalt kõrge rõhu all. Vastavalt SP XI-le on nendeks steriilsed vesi- ja mittevesilahused, suspensioonid, emulsioonid ja kuivained (pulbrid, poorsed massid, tabletid), mis lahustatakse vahetult enne manustamist steriilses lahustis. Parenteraalseks kasutamiseks mõeldud lahused mahuga 100 ml või rohkem klassifitseeritakse infusiooniks.
Sõltuvalt ravimite manustamiskohast eristatakse süste: intradermaalne, subkutaanne, intramuskulaarne, intravaskulaarne, intrakraniaalne, intraabdominaalne, intrapleuraalne, südamelihasesse jne. Igal juhtumil on oma manustamise spetsiifika. Raviainete süstimist kasutatakse laialdaselt kogu maailmas. See on seotud järgmisega positiivsed aspektid;
tegevuse kiirus;
doseerimistäpsus, sest ravimained ei hävine seedetraktis;
teadvuseta patsiendile ravimite manustamise võimalus;
selliste ravimite manustamine, mille puhul muud meetodid ei ole võimalikud, näiteks insuliinipreparaatide puhul;
ravimainete toime lokaliseerimise võimalus, mis on oluline intramuskulaarsete süstide jaoks;
võime kõrvaldada ravimainete ebameeldiva maitse ja lõhnaga seotud aistingud.
Samal ajal on süstimise meetodil negatiivneküljed:
Nakatumise oht, kuna manustatakse meditsiinilisi aineid, möödudes keha kaitsebarjääridest;
emboolia oht, st. veresoonte ummistus tahkete osakeste või õhumullide sattumise tõttu neisse;
füsioloogiliste häirete võimalus (osmootse rõhu pH muutus), mida keha valusalt tajub;
vajadus kvalifitseeritud meditsiinitöötajate järele.
Viimastel aastatel on välja töötatud valutu, nõelavaba ravimi manustamisviis, mis põhineb kõrge kineetilise energiaga ravimilahuse väga õhukese joa võimel kõrge rõhu all ületada kudede resistentsus ja tungida nendesse. See meetod on kuluefektiivne masssüstide, näiteks vaktsineerimiste puhul, ja seda on seni kasutatud piiratud määral.
5. Süstelahuste lahustid
Süstelahuste lahustid on süstevesi ja mittevesilahustid.
Vastavalt standardile FS 42-2620-97 peab süstevesi vastama kõikidele puhastatud vee nõuetele (FS 42-2619-97) ja olema pürogeenivaba.
Mittepürogeensus- see on pürogeensete ainete puudumine, mis põhjustavad intravaskulaarsel manustamisel keha palavikulist seisundit.
Pürogeensed ained võivad olla endogeensed ja eksogeensed (endo sees, ekso - väljaspool).
Endogeensed pürogeenid on raku- ja koeproduktid. Eksogeenseid pürogeene leidub mikroorganismides, peamiselt gramnegatiivsetes, ja need vabanevad nende elutegevuse käigus. Keemiliselt on pürogeensed ained mikroorganismide välismembraanide lipopolüsahhariidid või lipopolüsahhariid-valgu kompleksid.
Pürogeenide omadused
Fosfolipiidosa annab neile negatiivse laengu, nii et neid saab adsorbeerida positiivselt laetud filtreerivatele vaheseintele. Pürogeensed ained on mittelenduvad, neid ei destilleerita veeauruga, seetõttu on pürogeenivaba saamise peamine meetod destilleerimine veepiiskadest auruga puhastamisega.
Pürogeensed ained on väga stabiilsed, kuumakindlad ja hävivad ainult temperatuuril 250-300 °C 1-2 tunni jooksul.
Pürogeenide eemaldamiseks ravimilahustest kasutatakse adsorptsiooni alumiiniumoksiidil, kaoliinil, tärklisel, aktiivsöel, tselluloosil ja ka ioonivahetusvaikudel. Selle meetodi puudused hõlmavad ravimite samaaegset adsorptsiooni, eriti kivisöe kasutamisel, samuti vajadust puhastada depürogeenitud lahuseid mehaanilistest lisanditest.
Üks uusi tõhusaid viise lahuste pürogeenidest vabastamiseks on ultrafiltreerimine. See on lahuste eraldamise ja fraktsioneerimise protsess, mille käigus eraldatakse makromolekulid (m.m.-ga 1000 kuni 1 miljon) madala molekulmassiga ainete lahusest filtreerimise teel läbi membraanide. Näiteks ultrafiltrimisel läbi Vladilori membraanfiltri, mille pooride suurus on 100+25 A, säilib üle 99% pürogeenidest - lipopolüsahhariididest.
Vee hankiminejaoks süstid
Süstevett saab destilleerimise või pöördosmoosi teel.
Peamine saamise meetod - destilleerimine. Varustus jaoks seda meetodit- vee destilleerijad. Nende põhikomponendid on: aurusti, kondensaator ja kollektor. Pürogeenivaba vee saamiseks on vaja eraldada veepiisad aurufaasist. Sel eesmärgil kasutatakse erineva konstruktsiooniga spetsiaalseid seadmeid - eraldajaid. Need on tsentrifugaalsed, kiled, mahulised, kombineeritud. Tuleb meeles pidada, et kui vesi aurustis keeb, tekib mullide ja pinna aurustumine. Aurustis mullide aurustumisel tekivad keemise ajal seinalähedases kihis aurumullid. Need murduvad vedelikust välja, kannavad seda endaga kaasa ja muutuvad pisikesteks tilkadeks, mis on ebasoovitav, sest. tilgad võivad sisaldada pürogeenseid aineid. Pinna aurustumine väga õhukese kihina ei tekita tilka, seega on sobivam kasutada kileaurustit. Mullitavates seadmetes tuleks võimaluse korral keevkihi paksust vähendada. Ühtlase keemise tagamiseks on vaja ka kütet reguleerida. ja optimaalne aurukiirus.
Destillaadi kvaliteet paraneb veetöötluse kasutamisel, s.o. vee puhastamine enne destilleerimist, eemaldades sellest soolad, pindaktiivsed ained ja muud ained. See vähendab hinnakujundust, katlakivi kogust ja pikendab destilleerijate kasutusiga.
Vee destilleerijad
Apteegis saab süstevett seadmetes A-10 ja AEVS-4.25, 60.
Vee destilleerijad vee tootmiseksjaoks süstidtööstuslikes tingimustes
termokompressioonvee destilleerija. Selles aparaadis saadakse kvaliteetset pürogeenivaba vett, kuna esiteks toimub torude seintel õhukese kihina pinnaaurustumine ja teiseks takistab tilkade faasi kaasahaaramist piiskade suur kõrgus. aururuum. Seadme keerukuse tõttu on aga aparaat keeruline c. operatsiooni.
Finn-Aqua destilleerija. See masin toodab kvaliteetset süstevett aurude hoolika eraldamise ja pinna aurustamise teel. Seade on eelmisega võrreldes tehniliselt täiuslikum ja produktiivsem, sekundaarauru energia kulutatakse selles ratsionaalselt.
Vee saamine pöördosmoosi teel.
Pöördosmoos (või hüperfiltratsioon) on lahusti (vee) väljumine lahusest läbi poolläbilaskva membraani välise rõhu toimel. Soolalahuse ülerõhk on sel juhul palju suurem kui osmootne rõhk (р > π ). Rõhu erinevus p-π on pöördosmoosi liikumapanev jõud. Näiteks kui mereveel on osmootne rõhk p = 2,5 MPa, siis pöördosmoosi läbiviimiseks tuleb sellele anda välisrõhk 7-8 MPa.
Pöördosmoosi jaoks kasutatakse kahte tüüpi membraane: poorsed ja mittepoorsed.
Poorsed membraanid adsorbeerivad oma pinnal veemolekule. Sel juhul moodustub sorptsioonikiht, mille paksus on mitukümmend angströmit. Mittepoorsed membraanid moodustavad kontaktpinnal veemolekulidega vesiniksidemeid. Liigrõhu toimel need sidemed katkevad, veemolekulid difundeeruvad membraani vastassuunas - membraanikihi sees ja nende asemele tungivad järgmised. Soolad ja peaaegu kõik keemilised ühendid ei suuda läbi sellise membraani tungida, välja arvatud gaasid.
Süstevee saamise meetodite võrdlusdestilleerimise meetod. Eelised: kõrge puhastusaste, töökindlus, kuuma vee saamise võimalus, seadme auruga töötlemise võimalus. Puudused: kõrge hind, ebaökonoomne (suure energia- ja veekulu tõttu).
Pöördosmoosi meetod. Eelised: ökonoomsus. Puudused: mikroobse saastumise võimalus, membraanide sagedase asendamise vajadus (2-4 korda aastas).
Süstevee säilitamine
Eelistatav on kasutada värskelt valmistatud vett. Vee usaldusväärne säilitamine toimub spetsiaalsetes inertsest materjalist süsteemides, kus vesi on kõrgel temperatuuril (80-95 ° C piires) pidevas liikumises, s.o. ringleb ühest anumast teise ühtlase kiirusega. Süstevee maksimaalne kõlblikkusaeg aseptilistes tingimustes on 24 tundi.
Vee kvaliteeti hinnatakse järgmiste näitajate järgi: steriilsus, mittepürogeensus, pH, redutseerivate ainete olemasolu, süsinikanhüdriid, nitritid, nitraadid, kloriidid, sulfaadid, kaltsium ja raskmetallid. Ammoniaak ja kuivjääk - kehtestatud normide piires .
mittevesilahustid. Iseloomulik. Klassifikatsioon
Mittevesilahusteid kasutatakse:
Lahuste saamine vees lahustumatutest ainetest;
pikaajalise toimega lahenduste saamine;
lahenduste saamine pikaga säilitusaeg näiteks hüdrolüüsitavatest ainetest.
Nõuded mittevesilahustele:
mittetoksilisus;
kohaliku ärritava toime puudumine;
keemiline kokkusobivus ravimite ja abiainetega;
vastupidavus termilisele steriliseerimisele;
madal viskoossus.
Klassifikatsioonkeemilise olemuse järgi:
ühehüdroksüülsed alkoholid (etanool);
mitmehüdroksüülsed alkoholid (glütseriin, propüleenglükool);
estrid (etüüloleaat, bensüülbensoaat);
amiidid (metüülatseetamiid) jne.
Eraldatakse ka rasvõlisid, millest kõige sagedamini kasutatakse oliivi-, virsiku- jne.
Kasutatakse ka kompleksseid lahusteid. Nende hulka kuuluvad etanool, glütseriin, propüleenglükool, polüetüleenoksiid-400, bensiinalkohol jne.
Samuti tuleb märkida, et süstelahuste valmistamisel kasutatakse abiaineid: stabilisaatorid, säilitusained, solubilisaatorid (lahustuvust suurendavad ained). Abiainete arv on reguleeritud.